- 首页
- 资讯
Nature: 新加坡国立大学Ming Joo Koh课题组和牛津大学Benjamin G. Davis课题组实现天然糖的多样化转化
来源:化学加公众号 2024-06-20
导读:天然糖和碳水化合物含有许多具有类似反应性的羟基。因此,化学家通常依赖繁琐的多步骤保护基策略,将这些可再生原料转化为合成糖苷所需的糖给体。然而,直接将天然糖转化为复杂的糖苷仍然是一项重要的挑战。本文介绍了一种光诱导的方法,通过均裂(自由基)化学,实现了天然糖类化合物位点和立体选择性的糖基化,绕过了不必要的羟基保护和去保护。此过程类似于生物合成中通过区域控制生成瞬时糖基给体,然后在光激活下与亲电体进行自由基交叉偶联。通过对单糖和寡糖的异头位选择性官能化,这种无需保护基的“封端和糖基化(cap and glycosylate)”方法提供了获取一系列代谢稳定的糖基化合物的简便途径。由于糖给体的生物相容性,该方法还扩展到了直接蛋白质翻译后的糖基化修饰。

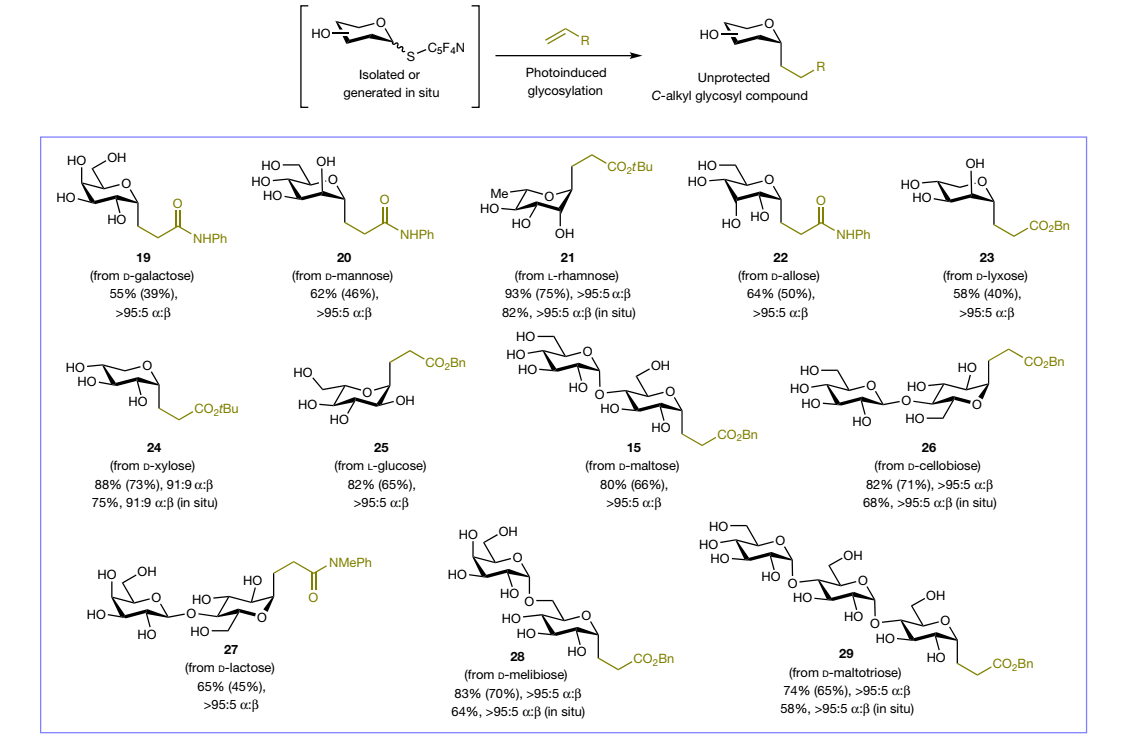
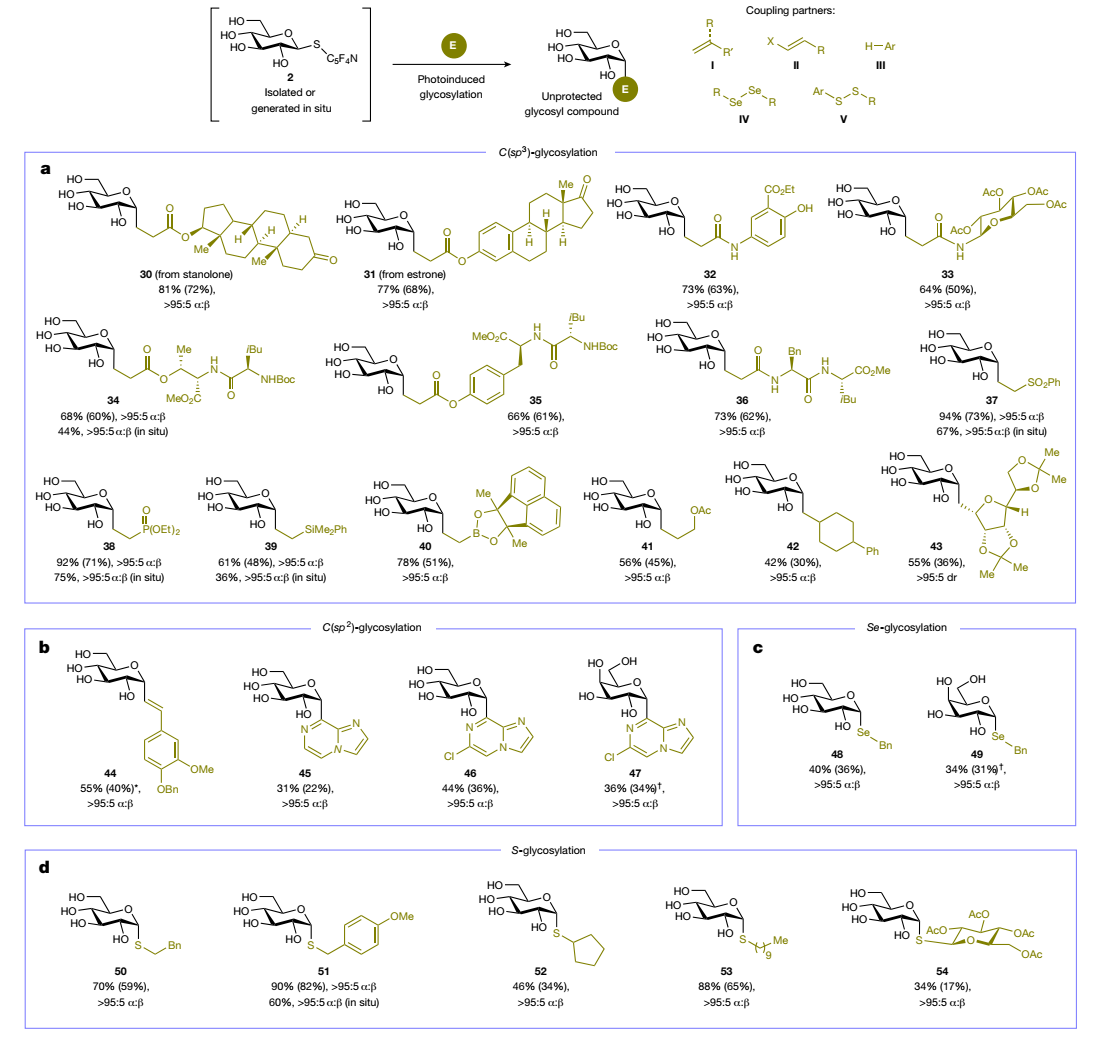
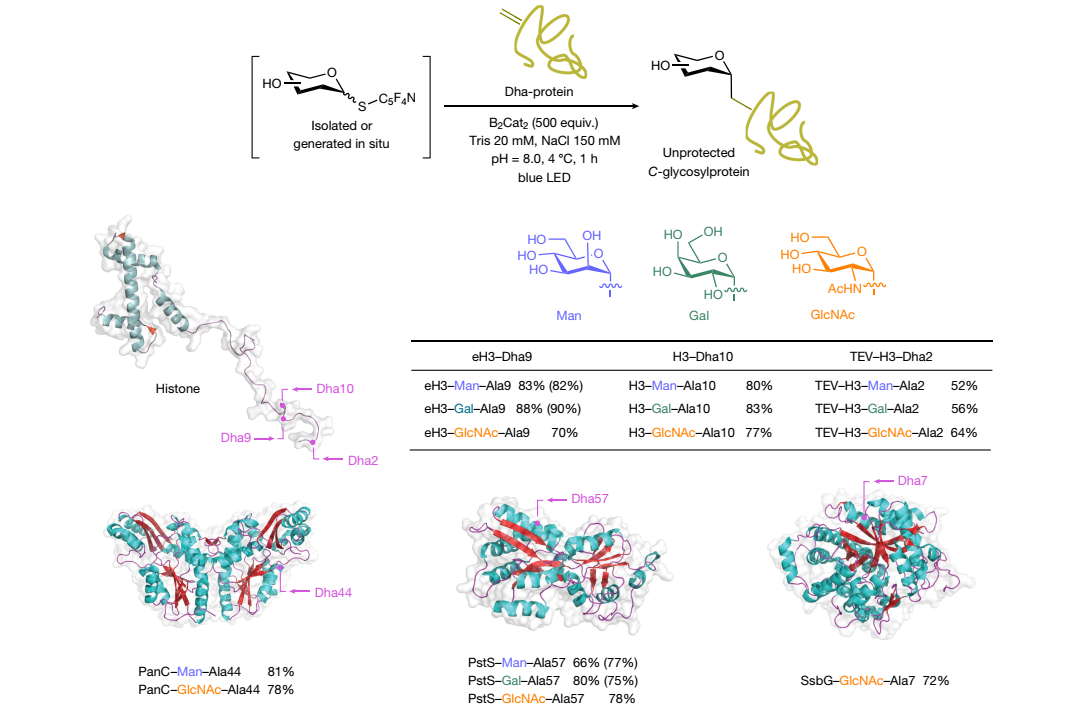
碳水化合物广泛分布于细胞中,并在许多生物过程中起着关键作用。自然界通常通过糖基化从而显著改变分子的功能。由于它们的重要性,人们投入了大量精力来获取这些糖类及其结合物,以更好地了解其性质、功能及其潜在的疾病相关作用,并推动糖类药物的发现。由于从自然界中提取纯样品的难度,化学家们主要通过合成手段来获得大多数糖类。为此,非酶化学糖基化提供了一条可靠的途径来合成大量天然和非天然糖苷实体。然而,与酶促反应可以通过使用无保护的多羟基糖基供体实现高效的区域控制糖基化不同,现有的化学糖苷化方法精度较低,通常需要繁琐的保护基策略来解决位点选择性问题。这些方法的复杂性在现有的合成C-糖苷化合物的途径中尤为突出。C-糖苷化合物在自然界中较为罕见,但作为O-糖苷的更稳定且生物活性更强的替代物,在开发治疗癌症、糖尿病和其他疾病的药物方面越来越受到重视。目前报道的非酶化学C-糖苷化通常需要多步反应序列(包括羟基保护、功能化和去保护),涉及精细的反应控制和/或苛刻的反应条件,以将完全无保护的天然糖(自然界中最丰富的形式)转化为包含异头位离去基团(如卤化物、酯、亚砜或砜)的糖基给体,进而通过碳-碳键形成反应生成所需的无保护C-糖苷化合物。与高度位点选择性的酶促C-糖苷化相比,这些方法的使用缺陷和低效率限制了它们在合成糖化学中的应用,尤其阻碍了其在复杂生物条件下的进一步应用。因此,建立一种能够直接耦合天然糖以进行广泛糖基化的反应模式,获取纯的立体异构体的C-糖苷化合物及其他水解稳定且具有重要药用价值的变体(如S-和Se-糖苷)以及C-连接的糖蛋白,一直是糖化学研究领域的重要目标。然而,由于效率、选择性和生物相容性等众多问题,一直未能实现该挑战。 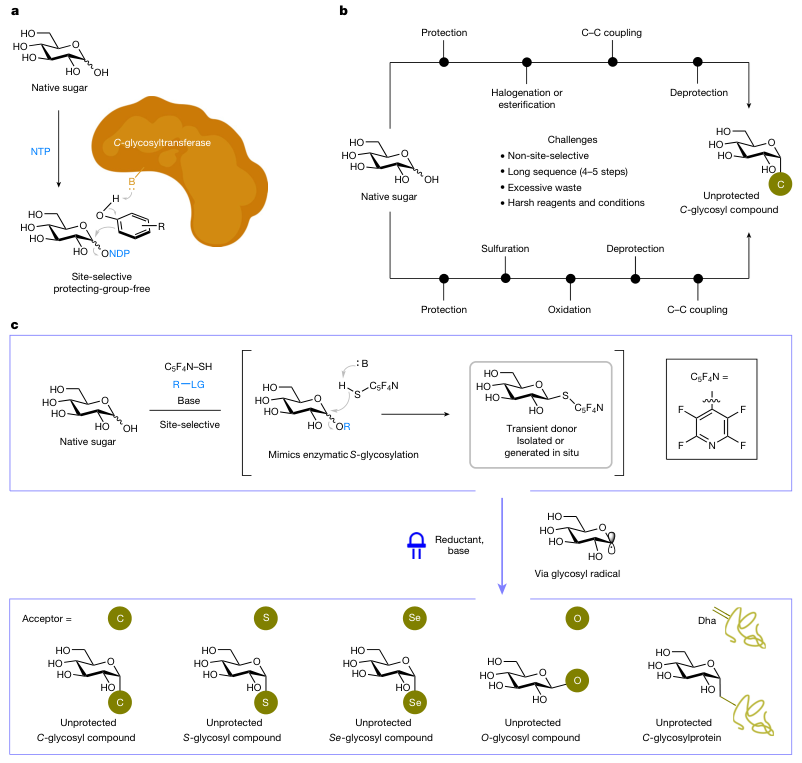 受生物合成S-糖苷化的启发,其中S-糖基转移酶通过区域选择性的糖基转移将端位磷酸化且无保护的核苷酸糖引入受体,从而形成稳定的S-糖苷键,作者推测可以采用仿生方法优先激活和取代天然糖的环状形式中的端位羟基(半缩醛)(cap)。这样可以得到一个硫代糖苷中间体,在适当条件下可以进行立体控制的单步操作进行脱硫交叉偶联,从而实现糖苷化(glycosylate)。就像在自然界中一样,临时生成的活化糖给体是无痕的。经过探索,作者发展了一种无金属且无需保护基的天然糖的转化反应,该方法通过温和的光照条件下与各种亲电体的自由基交叉偶联,解决了该领域的长期问题。该反应可用于高效制备C-糖苷、S-糖苷Se-糖苷化合物以及O-糖苷。更重要的是,该方案适用于直接化学合成无保护的C-糖蛋白,这种翻译后修饰方法补充了类似的生物O-和N-糖基化过程。 在获得最优条件,并且经过较为充分的机理研究后。作者首先对各种天然糖在标准条件下的适用性展开了考察。发现各种天然糖所衍生的糖给体在该反应条件下均有着较好的适用性,能以较高的收率和良好到优异的立体选择性制备目标C-糖苷产物。这其中包括了常见的天然糖(19-21, 24),稀有糖(22-23),非天然糖(25),二糖(15,26-28)和寡糖(29)。此外,作者对亲电偶联试剂的底物适用性进行了探索,多种生物活性分子和短肽衍生的丙烯酸类化合物都有着较好的适用性(30-36)。其他不同类型的Michael受体也都有着较好的底物适用性(37-40),以及几种非活化烯烃在标准条件下均有良好的底物适用性(41-43)。值得一提的是,烯集卤代物、杂环芳烃、二硒化物和二硫化物都能以高立体选择性获得相应的无保护C-烯基(44)、C-杂芳基(45-47)、Se-(48、49)和S-(50-54)糖苷化合物。通过简单的条件调整,苯酚类化合物作为受体以中等产率(17-43%)和>95:5 β:α选择性获得相应的O-糖苷化合物(55-59)。糖蛋白在生物学领域具有广泛应用,由于糖蛋白在生物体内的广泛存在,解锁糖蛋白的生物学功能一直是化学生物学领域中的重点及难点问题。然而,由于蛋白翻译后糖基化过程的可逆性,为进一步研究糖蛋白的生物功能带来挑战。若能通过化学方法获取对于糖基水解酶稳定的C-糖蛋白,这将可能为研究生物体内O/N-糖蛋白的生物学功能提供新的思路。经过对反应条件进行重新改造,作者实现了在水相对多种蛋白的选择性糖基化反应。该反应具有优异的普适性和生物相容性,可用于大小和折叠形式不同的蛋白底物。 新加坡国立大学Ming Joo Koh课题组和牛津大学Benjamin G. Davis课题组利用“封端-糖基化(cap and glycosylate)”策略在光诱导下实现了天然糖类化合物位点选择性和立体选择性的多样性转化,以高产率、高区域选择性和立体选择性获得了一系列无保护C-、S-、Se-和O-糖苷化合物。此外,作者还将该方法应用于蛋白质的直接翻译后糖基化,进一步展现出该方法的实用性和该新型糖给体优异的生物相容性。论文第一作者为Ming Joo Koh组博士生蒋仪,共同第一作者为博士后魏怡。
受生物合成S-糖苷化的启发,其中S-糖基转移酶通过区域选择性的糖基转移将端位磷酸化且无保护的核苷酸糖引入受体,从而形成稳定的S-糖苷键,作者推测可以采用仿生方法优先激活和取代天然糖的环状形式中的端位羟基(半缩醛)(cap)。这样可以得到一个硫代糖苷中间体,在适当条件下可以进行立体控制的单步操作进行脱硫交叉偶联,从而实现糖苷化(glycosylate)。就像在自然界中一样,临时生成的活化糖给体是无痕的。经过探索,作者发展了一种无金属且无需保护基的天然糖的转化反应,该方法通过温和的光照条件下与各种亲电体的自由基交叉偶联,解决了该领域的长期问题。该反应可用于高效制备C-糖苷、S-糖苷Se-糖苷化合物以及O-糖苷。更重要的是,该方案适用于直接化学合成无保护的C-糖蛋白,这种翻译后修饰方法补充了类似的生物O-和N-糖基化过程。 在获得最优条件,并且经过较为充分的机理研究后。作者首先对各种天然糖在标准条件下的适用性展开了考察。发现各种天然糖所衍生的糖给体在该反应条件下均有着较好的适用性,能以较高的收率和良好到优异的立体选择性制备目标C-糖苷产物。这其中包括了常见的天然糖(19-21, 24),稀有糖(22-23),非天然糖(25),二糖(15,26-28)和寡糖(29)。此外,作者对亲电偶联试剂的底物适用性进行了探索,多种生物活性分子和短肽衍生的丙烯酸类化合物都有着较好的适用性(30-36)。其他不同类型的Michael受体也都有着较好的底物适用性(37-40),以及几种非活化烯烃在标准条件下均有良好的底物适用性(41-43)。值得一提的是,烯集卤代物、杂环芳烃、二硒化物和二硫化物都能以高立体选择性获得相应的无保护C-烯基(44)、C-杂芳基(45-47)、Se-(48、49)和S-(50-54)糖苷化合物。通过简单的条件调整,苯酚类化合物作为受体以中等产率(17-43%)和>95:5 β:α选择性获得相应的O-糖苷化合物(55-59)。糖蛋白在生物学领域具有广泛应用,由于糖蛋白在生物体内的广泛存在,解锁糖蛋白的生物学功能一直是化学生物学领域中的重点及难点问题。然而,由于蛋白翻译后糖基化过程的可逆性,为进一步研究糖蛋白的生物功能带来挑战。若能通过化学方法获取对于糖基水解酶稳定的C-糖蛋白,这将可能为研究生物体内O/N-糖蛋白的生物学功能提供新的思路。经过对反应条件进行重新改造,作者实现了在水相对多种蛋白的选择性糖基化反应。该反应具有优异的普适性和生物相容性,可用于大小和折叠形式不同的蛋白底物。 新加坡国立大学Ming Joo Koh课题组和牛津大学Benjamin G. Davis课题组利用“封端-糖基化(cap and glycosylate)”策略在光诱导下实现了天然糖类化合物位点选择性和立体选择性的多样性转化,以高产率、高区域选择性和立体选择性获得了一系列无保护C-、S-、Se-和O-糖苷化合物。此外,作者还将该方法应用于蛋白质的直接翻译后糖基化,进一步展现出该方法的实用性和该新型糖给体优异的生物相容性。论文第一作者为Ming Joo Koh组博士生蒋仪,共同第一作者为博士后魏怡。文献详情:
Direct radical functionalization of native sugars.Yi Jiang, Yi Wei, Qian-Yi Zhou, Guo-Quan Sun, Xia-Ping Fu, Nikita Levin, Yijun Zhang, Wen-Qiang Liu, NingXi Song, Shabaz Mohammed, Benjamin G. Davis* & Ming Joo Koh*.https://doi.org/10.1038/s41586-024-07548-0
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn