(图片来源:Angew. Chem. Int. Ed.)
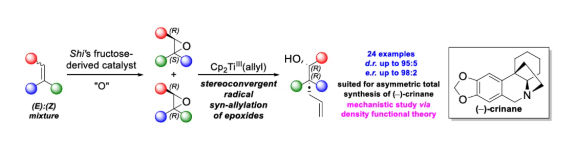
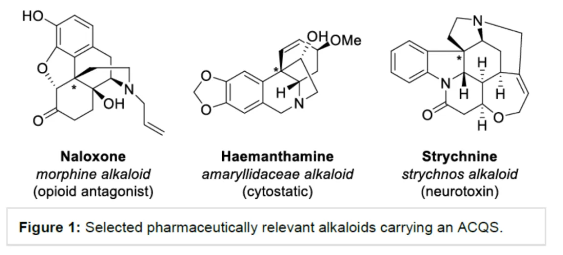
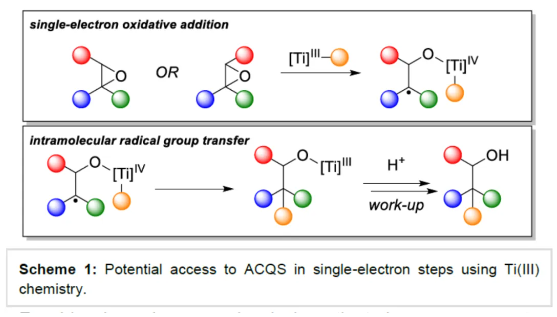
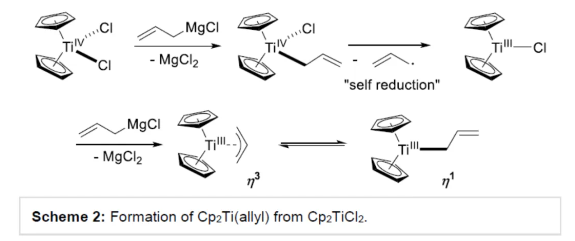
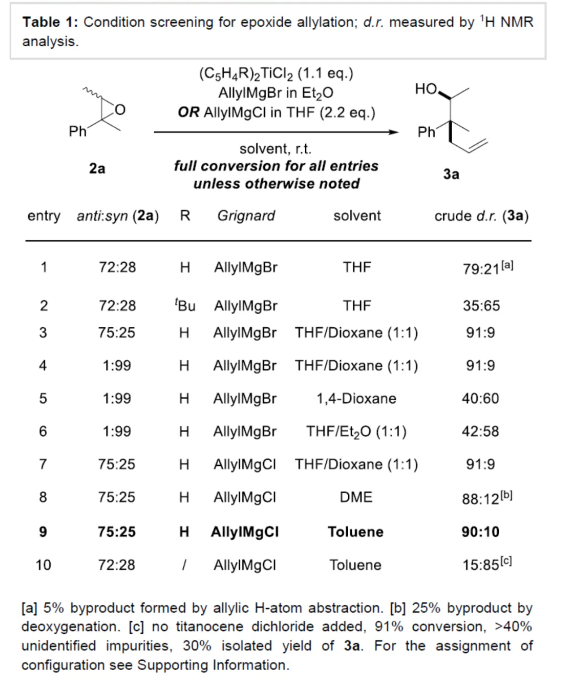
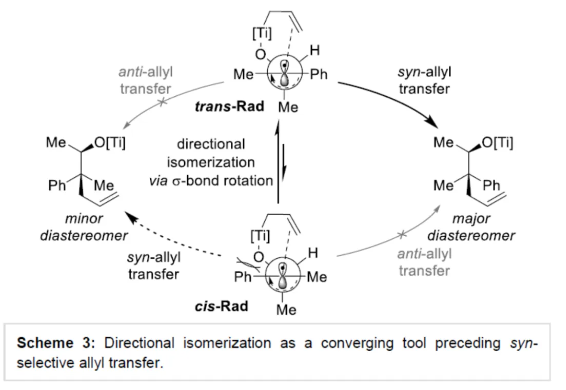
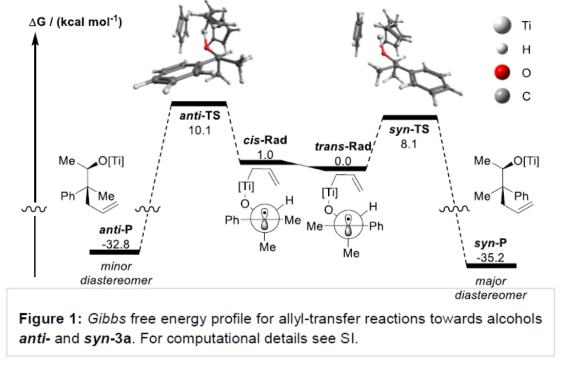
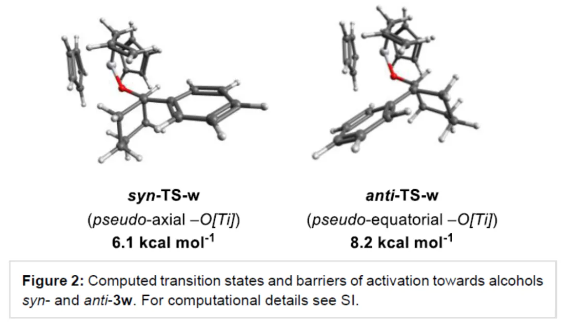
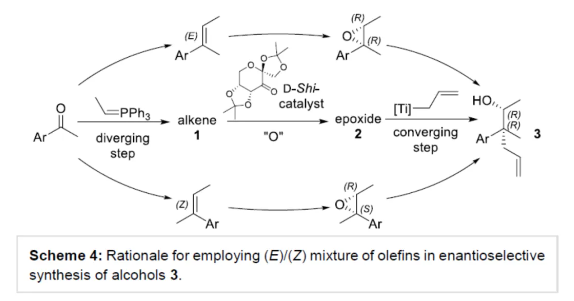
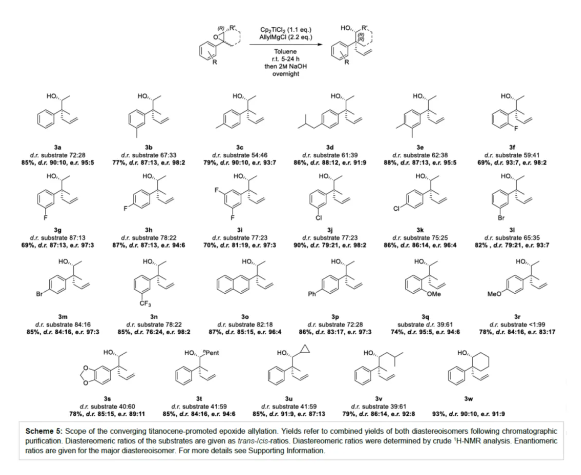
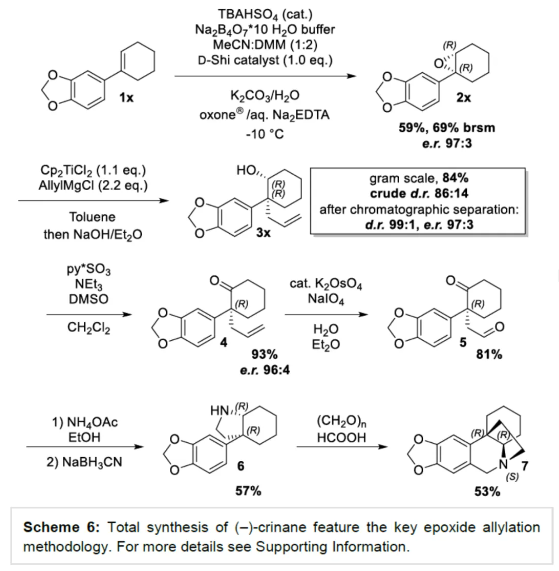
季碳手性中心(ACQS)是一个重要的结构单元,广泛存在于天然产物和生物活性分子等中,如吗啡、amaryllidaceae以及strychnos生物碱(Figure 1)。然而,高效与对映选择性构建全季碳季碳手性中心,仍然具有挑战。 (图片来源:Angew. Chem. Int. Ed.)虽然二级和三级手性中心可以通过各种对映选择性羰基还原或α-官能团化方法获得,但全碳手性中心的构建通常需要更精细的方法,如1,3-置换反应、烯醇碳酸酯烯丙基化、环加成反应、共轭加成、去对称化反应以及使用二烯、联烯或氧化异戊二烯通过瞬态烯丙基铱配合物的转移加氢羰基烯丙基化反应等。此外,使用通常构象不稳定的自由基可以为ACQS的合成提供一种替代策略,从而减轻对立体定义底物的需求(Scheme 1)。作者设想,采用环氧化物的非对映混合物作为ACQS前体,通过自由基机理可进行官能团转移。2023年,张永强课题组(J. Am. Chem. Soc. 2023, 145, 21122.)报道了首例环氧化物的自由基烯丙基化反应,合成了对映体富集的ACQS。近日,德国波恩大学Andreas Gansäuer与Zheng-Wang Qu课题组开发了一种使用Cp2Ti(III)allyl作为双功能试剂,通过电子转移进行环氧化物开环后生成烯丙基二茂钛(allyltitanocene)自由基。其与二茂钛氢化物的分子内氢原子转移类似,随后从金属到自由基中心的分子内烯丙基转移具有高度的立体选择性。由于自由基的生成伴随着自由基中心的构型损失,因此该过程可以使用环氧化物非对映异构体的混合物。 化学加——科学家创业合伙人,欢迎下载化学加APP关注。 (图片来源:Angew. Chem. Int. Ed.)首先,作者以市售的Cp2TiCl2和allylMgBr直接原位制备Cp2Ti(allyl)(Scheme 2)。这种非常方便的制备方法可能是通过烯丙基从Mg到Ti的转金属化形成的Ti(IV)–烯丙基键的均裂来进行的。(图片来源:Angew. Chem. Int. Ed.)其次,作者以外消旋环氧化物2a作为模型底物,进行了相关反应条件的筛选(Table 1)。当以外消旋环氧化物2a(anti : syn为75:25)为底物,allylMgBr(2.2 eq.)作为格氏试剂,Cp2TiCl2(1.1 eq.)作为催化剂,在甲苯溶剂中室温反应12 h,可以85%的收率得到产物3a,d.r.为90:10,e.r.为95:5。 (图片来源:Angew. Chem. Int. Ed.)3a形成的合理机理是通过2a与Cp2Ti(III)(allyl)的配位进行,随后的单电子氧化加成形成更高取代的β-titanoxy自由基trans-Rad和cis-Rad,它们通过定向异构化(directional isomerization)而平衡,以形成更稳定的旋转异构体(rotamer)trans-Rad,取代基之间的空间排斥最小。随后,通过七元过渡态的分子内、syn-选择性以及自由基烯丙基转移,从而确认ACQS的构型(Scheme 3)。 (图片来源:Angew. Chem. Int. Ed.)同时,作者还进行了相关的理论计算(Figure 1)。由于环张力的释放以及由较弱Ti-C键形成强C-C键,整个自由基烯丙基化是一个高度放热的过程。环氧化物2a是区域选择性开放的。有趣的是,苄基自由基trans-Rad仅比cis-Rad稳定1.0 kcal mol-1。这是Ph-取代基与醇盐结合的烯丙基环戊二烯钛的空间相互作用增加的结果。同时,烯丙基化过程构成了一个协同的SH2'反应。从两种过渡态的活化能可以清楚地看出,选择性是由活化焓的差异决定的。 (图片来源:Angew. Chem. Int. Ed.)此外,计算研究表明,2w的烯丙基化的立体化学过程由环己烷在两个双环过渡态的构象平衡决定(Figure 2)。与SH2反应的五元过渡态相比,自由基烯丙基化的非对映体过渡态的环状七元结构具有更大程度的结构灵活性,因此,预期立体选择性略有降低。 (图片来源:Angew. Chem. Int. Ed.)随后,作者发现,采用(E)/(Z)-烯烃作为底物,同样可对映选择性合成手性醇产物3,涉及史一安环氧化与Ti(III)-促进的环氧化物的分子内自由基转移烯丙基化的过程(Scheme 4)。(图片来源:Angew. Chem. Int. Ed.)紧接着,作者对底物范围进行了扩展(Scheme 5)。首先,当底物中的芳基上含有烷基、卤素、三氟甲基、苯基等时,均可顺利反应,获得相应的产物3a-3s,收率为69-90%,d.r.为79:21-95:5,e.r.为83:17-98:2。其次,当底物中的R’为正辛基、环丙基与异丙基时,也与体系兼容,获得相应的产物3t-3v,收率为79-85%,d.r.为84:16-91:9,e.r.为87:13-94:6。此外,含有环己基稠合的环氧化物,也是合适的底物,可以93%的收率得到产物3w,d.r.为90:10,e.r.为91:9。 (图片来源:Angew. Chem. Int. Ed.)最后,作者对反应的实用性进行了研究(Scheme 6)。以烯烃1x为初始底物,经史一安环氧化反应,可以59%的收率得到环氧化物2x,e.r.为97:3。环氧化物2x在上述标准条件下进行分子内自由基转移烯丙基化反应,可以84%的收率得到醇化合物3x,d.r.为86:14。通过进一步的柱色谱纯化,可将d.r.提高至99:1,e.r.为97:3。醇化合物3x经Parikh-Doering氧化反应,可以93%的收率得到酮化合物4,e.r.为96:4。酮化合物4的端烯经氧化断裂,可以81%的收率得到醛化合物5。醛化合物5经双重还原胺化,可以57%的收率得到二级胺化合物6。二级胺化合物6经Pictet-Spengler反应,可以53%的收率得到(–)-Crinane(7)。 (图片来源:Angew. Chem. Int. Ed.)德国波恩大学Andreas Gansäuer与Zheng-Wang Qu课题组报道了一种新型的Ti(III)-促进的环氧化物的分子内自由基转移烯丙基化反应,其特征是定向异构化步骤,合成了一系列高度非对映体和对映体富集的α-季碳醇衍生物。该策略的成功与之前的 (E)/(Z)-烯烃混合物的史一安环氧化生成两种非对映异构的环氧化物有关,这两种环氧化物都是高度富集对映异构体。这种独特的方法可将两种环氧化物相互转化,生成含有全碳季碳手性中心的单一产物。此外,通过对生物碱(–)-Crinane的全合成,进一步证明了反应的实用性。 文献详情:
Sebastian Höthker, Annika Plato, Stefan Grimme, Zheng-Wang Qu, Andreas Gansäuer*. Stereoconvergent Approach to the Enantioselective Construction of α-Quaternary Alcohols by Radical Epoxide Allylation. Angew. Chem. Int. Ed. 2024, https://doi.org/10.1002/anie.202405911