- 首页
- 资讯
JACS:厦大徐海超团队光电不对称催化(PEAC)
来源:化学加原创 2023-08-21
导读:近日,厦门大学徐海超教授课题组在Journal of the American Chemical Society上报道了光电不对称催化新方法,实现了不对称烯烃杂芳基氰化反应,文章链接:doi.org/10.1021/jacs.3c07146,该论文第一作者为厦门大学化学化工学院2023届博士赖小丽。
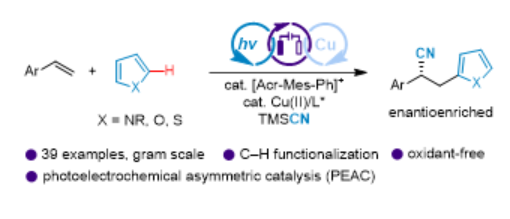
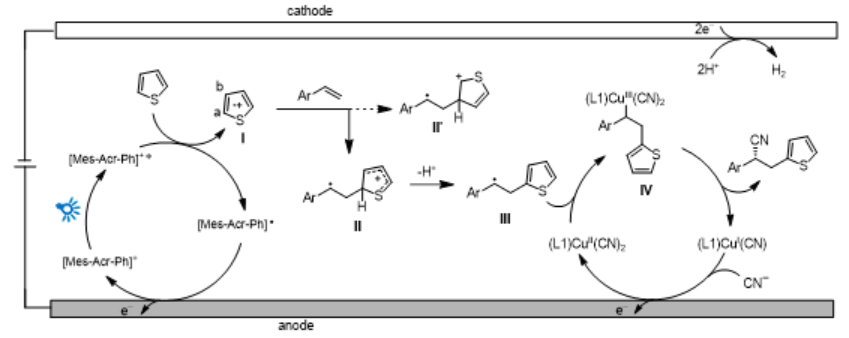
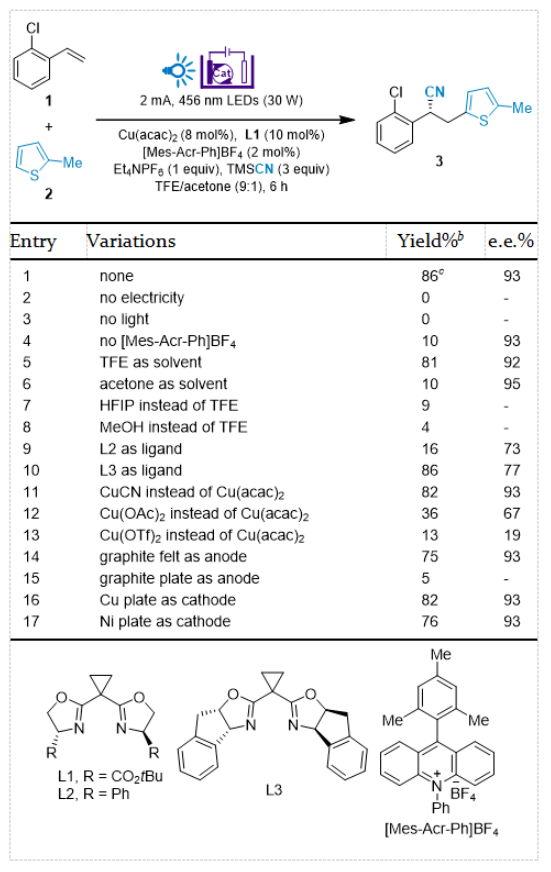
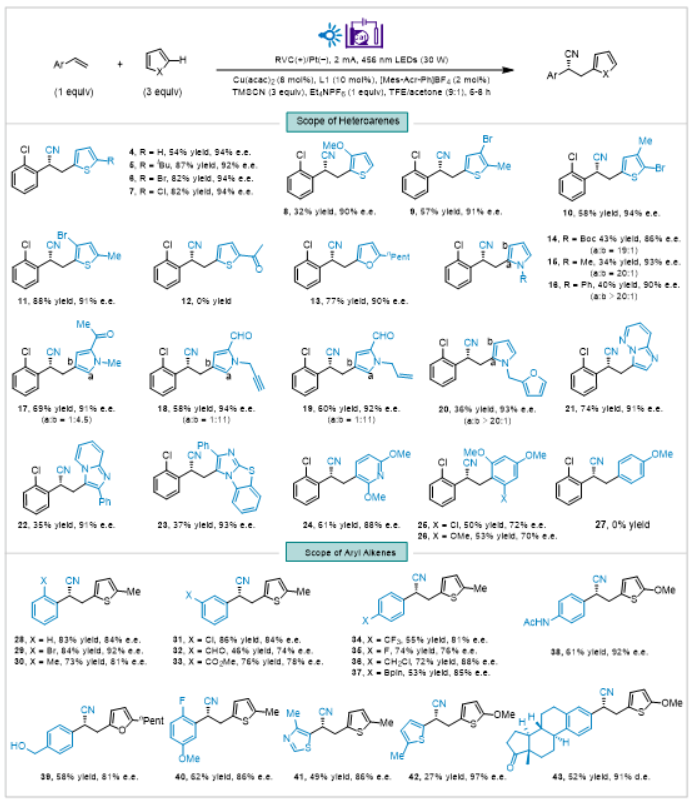
过去十几年,随着环保意识的提升和对合成效率及其可持续性的需求日增,光催化和有机电合成因其绿色、安全的特性,得到了显著的发展,逐渐成为有机化学研究的两个焦点。将这两个领域结合在一起,一个新的研究领域——分子光电催化(molecular photoelectrocatalysis)就应运而生。该领域集光催化和电合成的优点于一身,分子光电催化模式下能够触及更广泛的氧化还原电势,使得在更温和的电极电势下进行氧化还原反应成为可能。在2022年,光电不对称催化(Photoelectrochemical Asymmetric Catalysis, PEAC)方法被首次报道(Nat. Catal.2022, 5, 943; J. Am. Chem. Soc.2022, 144, 21674),尽管光电不对称催化是最新的发展,但它已经在扩展不对称C-H氰基化的应用范围上发挥了关键的推动作用,并且还推动了直接不对称脱羧氰基化的发展(J. Am. Chem. Soc.2022, 144, 20201; Chem. Sci.2023, 14, 705; Chem. Eur. J.2023, 29, e202203962.)。下载化学加APP到你手机,更加方便,更多收获。图1. 光电催化不对称烯烃C–H杂芳氰化(图片来源:J. Am. Chem. Soc.)手性腈是生物活性化合物的重要结构单元,也是用途广泛的合成中间体。在制备手性腈的各种方法中,烯烃的对映选择性自由基氰基化已经成为一种有效的策略。然而现有的烯烃碳氰化反应需要使用预官能团化的碳自由基前体。其中烯烃的不对称芳氰化更是被证明是一项艰巨的任务,已有的唯一方法必须使用具有潜在危险的芳基重氮盐试剂。徐海超课题组迎难而上,通过使用他们团队发展的分子光电不对称催化方法,通过C–H官能团化实现了烯烃的对映选择性杂芳氰化。该方法采用吖啶鎓盐和手性铜络合物作为催化剂,通过芳基自由基阳离子过程,高效地将容易获得的芳基烯烃和未官能团化的杂芳烃转化为对映体富集的腈。这一突破不仅为有用的结构提供了新的合成策略,而且有望加快分子光电催化的发展,为创新和进步打开更多大门。图2. 反应可能机理(图片来源:J. Am. Chem. Soc.)首先,作者以芳基烯烃1和噻吩2作为模型底物,进行了条件筛选和优化,得出了最优反应条件:456 nm LED为光源,2mA为反应电流,市售的[Mes-Acr-Ph]BF4和Cu(acac)2为催化剂,手性双噁唑啉配体L1作为配体,TFE/Acetone(9:1)的混合溶剂作为反应溶剂,TMSCN为氰基源。在最优条件下反应6小时,能以86%的分离收率,93%的ee得到目标产物3。图3. 反应条件筛选与优化(图片来源:J. Am. Chem. Soc.)得到最优条件后,作者考察了该反应的底物范围。结果表明,该方法与噻吩(4)及其衍生物兼容,例如在噻吩2号位上带有tBu(5)、Br(6)或 Cl(7)以及在噻吩3号位上含有 MeO(8)的衍生物。带有双官能团的噻吩(9-11)和2-戊基呋喃(13),在该反应中也具有良好的产率和对映选择性。而氧化电势高于芳基烯烃1(Ep/2ox = 2.00 V vs SCE)的2-乙酰基噻吩(Ep/2ox = 2.19 V vs SCE)未能生成目标产物12。值得一提的是,受杂芳基自由基阳离子中间体稳定性的影响,当吡咯的氮原子上带有Boc(14)、Me(15)或 Ph(16)基团时,可以选择性地在2位发生反应。相反,当吡咯2位被羰基取代时,则有利于在4位上发生反应(17-19)。此外,含有一个活性吡咯环和一个呋喃环的底物只在更富电子的吡咯环上发生反应(20)。其他兼容且具有极佳区域选择性的杂芳烃包括咪唑并[1,2-b]哒嗪(21)、咪唑并[1,2-a]吡啶(22)、苯并[d]咪唑并[2,1-b]噻唑(23)和 2,6-二甲氧基吡啶(24)。富电子的取代苯,如1-氯-3,5-二甲氧基苯(25)和 1,3,5-三甲氧基苯(26)也可以发生区域选择性反应,但只有中等程度的对映选择性。另一方面,该反应也可以很好地兼容各种芳基烯烃。苯环邻位可以被H(28)、Br(29)和Me(30)取代,间位可以被Cl(31)、CHO(32)和CO2Me(33)取代,对位可以被CF3(34)、F(35)、CH2Cl(36)、硼酸酯(37)、AcNH(38)和 CH2OH(39)取代。该方法还适用于1,4-二取代苯环(40)。其他芳香环,如噻唑(41)或噻吩(42)也可替代苯环。此外,雌酮衍生物也可以很好地反应,以良好的收率和对映选择性得到烯烃双官能团化产物(43)。图4. 底物扩展(图片来源:J. Am. Chem. Soc.)为了进一步说明分子光电不对称催化方法的合成效用,作者进行了克级规模放大,以74%的收率,92%的对映选择性得到了1.36克的目标产物3。实验结果证明3的CN基团可以在不影响对映选择性的情况下转化为酰胺(44)、酯(45)以及氨基甲基(46)。图5. 放大与转化(图片来源:J. Am. Chem. Soc.)厦门大学徐海超教授课题组成功开发了一种新型分子光电催化技术,利用C–H官能团化,对烯烃进行了不对称杂芳氰化。该反应的关键在于分子光电催化和不对称铜催化的串联催化。文献详情:
Xiao-Li Lai and Hai-Chao Xu*. Photoelectrochemical Asymmetric Catalysis Enables Enantioselective Heteroarylcyanation of Alkenes via C–H Functionalization. J. Am. Chem. Soc. 2023, https://doi.org/10.1021/jacs.3c07146
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn