

1 月 8 日,2022 年国家医保药品目录谈判工作正式结束,Paxlovid 因辉瑞报价高未能成功。
Paxlovid 于去年 2 月在国内获批上市,曾以 2300 元/盒的价格被临时纳入医保,后又下调至 1890 元/盒,综合上医保报销后患者最低自付为 189 元/盒。
在谈判失败后,医保仍将临时性支付到 2023 年 3 月 31 日,也就是说,自 4 月 1 日起,患者购买 Paxlovid 需要自费
医保谈判失败,国内暂无仿制药
一般来说,在医保谈判过程中,如果企业确认后的价格高于医保方谈判底价的 115%,则谈判失败,自动终止。双方最终提出的价格未公布,辉瑞公司的首席执行官 Albert Bourla 表示,「中国要求的价格低于辉瑞对大多数中低收入国家的价格...中国是世界第二大经济体,我认为他们支付的费用不应低于部分国家」。
去年 8 月,浙江华海药业公告宣布,与辉瑞签订了《生产与供应主协议》, 华海药业将在 5 年内为 Paxlovid 提供制剂委托生产服务,由辉瑞提供奈玛特韦原料药与利托那韦制剂,华海药业负责奈玛特韦制剂生产,并完成组合包装。
今年 1 月 10 日,有投资者向华海药业提问,「请问华海现在有生产辉瑞新冠药品吗?除了在国内合作,双方有在国外市场合作代工生产吗?」
图源:中国经济网
浙江华海药业股份有限公司在互动平台表示,公司正积极配合辉瑞加速推进Paxlovid本土化项目的各项工作,以满足中国患者的新冠治疗需求。

华海药业初创于1989年,其前身为临海市汛桥合成化工厂,2001年1月整体变更设立为浙江华海药业股份有限公司。2003年3月,公司股票在上海证券交易所成功上市。浙江华海药业股份有限公司是国家级高新技术企业、国家创新型企业和省政府确认的“五个一批”重点企业,设有国家级企业技术中心、博士后科研工作站,是全国首家荣获“国家环境友好企业”称号的医药企业。2000—2008年连续九年名列“浙江省医药工业十强企业”。
2019年浙江高新企业百强榜排名第84位。2020年3月18日,华海药业以280亿元人民币市值位列《2020胡润中国百强大健康民营企业》第52。
公司现有员工7000余人,在全球拥有40多家分子公司(包括中国、美国、日本、德国等);主要业务覆盖化学药、生物药、医药包装、贸易流通等多个领域,与全球800多家制药企业建立了长期合作关系,为100多个国家和地区提供医疗健康产品。

此前,据彭博社消息称,辉瑞公司首席执行官艾伯乐(Albert Bourla)当地时间周一表示,中国市场对Paxlovid的需求猛增,导致供应紧张,他正在与中国的合作伙伴合作,从今年上半年开始在中国提供新冠口服药Paxlovid。他当日在旧金山举行的摩根大通医疗保健会议上透露,该合作伙伴的生产尚未开始,但很快会启动,“即使在未来3~4个月内就实现这个目标,我也不会感到意外。”不过他并未透露相关公司名称。
去年,A股原料药龙头华海药业(600521.SH)拿下了辉瑞Paxlovid的制剂委托生产协议,由华海药业在协议期内为辉瑞在中国大陆市场销售的Paxlovid提供制剂委托生产服务。其中,辉瑞提供奈玛特韦原料药与利托那韦制剂,华海药业负责奈玛特韦制剂生产,并完成组合包装。
1月9日,华海药业在回应媒体时称,目前公司在加速推进辉瑞产品本地化生产项目的各项工作,以保障Paxlovid在中国市场的充足供应,但目前Paxlovid本土化还没有批下来。
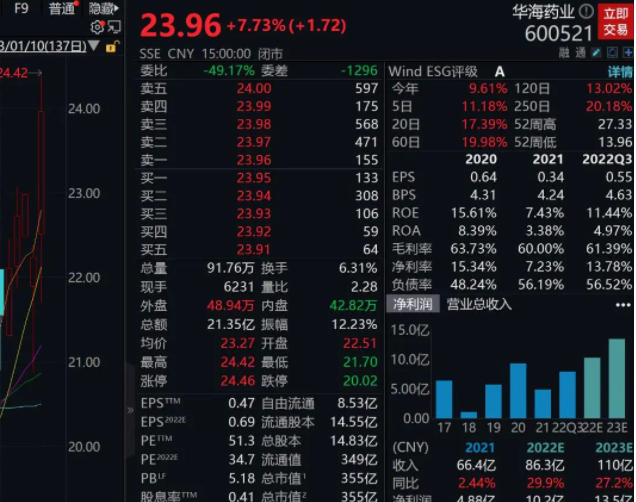
截至收盘,华海药业(600521.SH)涨近8%,报23.96元/股,总市值355亿元。
那么,Paxlovid要从进口产品转为本地化生产,需要经过哪些程序?这一过程大致需要多久完成?
我国目前实行MAH制度(药品上市许可持有人),何时进行生产取决于辉瑞何时拿到本地化生产许可证。
俄罗斯工程院外籍院士、昆翎医药联合创始人张丹向记者表示,辉瑞之所以选择进口转地产,是因为在国内生产可能会大幅降低成本。对于辉瑞而言,要实现在中国的本地化生产有两种路径选择。一是由辉瑞的在华子公司为代理;二是选择合作伙伴,例如华海药业为代理。
上述业内人士进一步分析,前一种方式为辉瑞自己的子公司持证,相当于华海药业仅赚取Paxlovid的加工费。而后者相当于辉瑞和华海药业的BD(商务拓展)合作,辉瑞将Paxlovid的相关专利、生产工艺、质量体系等都转卖给华海药业,由华海药业生产Paxlovid后,获取销售分成。
此前,1月9日,华海药业投资者关系部门相关人士在回应媒体时称,“医保是辉瑞在谈,公司只是给辉瑞做代工”。不过,上述业内人士认为,仅从商业合作的角度上看,选择后者的方式对辉瑞而言更加方便。因为按照现行规定,持证方需要自行负责产品的质量体系,放行检测等工作不可以外包。换而言之,授权给合作伙伴对于辉瑞而言减少了一些工作。而张丹指出,选择何种方式是出于公司的整体战略考量,外部人士难以预测。
在决定本地化生产方式后,辉瑞与合作伙伴还需要完成进口API(原料药)登记和补充产品验证性数据。这是为了来验证转为本地生产的产品与原来的进口产品是否完全一致,包括转交本地生产的API处方、生产工艺、质量系统等是否一致,本地生产的产品与进口产品在临床上的药效、安全性是否存在差异等。具体而言,对于一些结构简单、稳定、合成过程并不复杂的化药来说,通过溶出试验等体外试验就足以完成这一过程。而对于一些结构不稳定、合成工艺复杂、缓释制剂、吸入式药物等,则可能需要做临床试验。前者花费的时间一般在3至6个月,后者则相对繁琐,涉及临床批件、伦理审查等,需要半年至一年。
对于比对试验,上述业内人士认为,Paxlovid可能仅需完成体内外相关性(IVIVC)评价即可。其与验证性临床试验的区别在于,IVIVC评价入组的是健康人群,验证性临床试验入组的是相关患者。因此IVIVC评价完成难度更小、速度更快。但其认为,无论补充何种试验,由于Paxlovid的半衰期本身就很短,因此这一过程不会花很长时间。业内人士认为,若辉瑞的合作伙伴,如华海药业的工艺验证、清洁验证等都没有问题,也有空置的生产线专门用来生产相关产品,预计从申报到上市的时间大约在三到四个月。
香港大学李嘉诚医学院生物医学学院、病毒学专家金冬雁教授表示,Paxlovid患者在感染后的72小时内服用效果最好,若出现重症就没有太大价值,数据显示该药对65岁以上老人及有基础病的患者较为有效,能降低81%死亡率,但40-64岁年龄组没有明显获益。
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn