

氮杂环丙烷类化合物是一类重要的小环杂环化合物,在天然产物和药物中具有重要作用。之前报道的氮保护的氮杂环丙烷硅化的方法主要通过与硅亲电试剂的非催化转金属化过程实现。Jørgensen课题组通过铜催化三甲基硅基重氮甲烷和亚胺的[2+1]环加成反应首次实现了对该底物的催化不对称合成,但效果不佳。另外,Ooi课题组通过NHC催化实现了对C-硅基化含氮环丙烷外消旋混合物的动力学拆分。从已知方法来看,不饱和含氮三元环的亲核加成反应是可行的,但目前还没有关于硅亲核试剂对2H-吖丙因不对称加成的报道。
2H-吖丙因类化合物可被视为环亚胺,其3-取代衍生物为低活性酮亚胺。作者、Sato和何伟课题组分别以Si-B试剂作为硅亲核试剂的来源,开发了铜催化对醛亚胺的硅基化不对称加成反应。只有何伟课题组的反应体系适用于反应性较低的酮亚胺,虽然反应的对映选择性较好但产率较低。因此,对酮亚胺进行硅基化不对称加成的反应体系还有待进一步的探索。
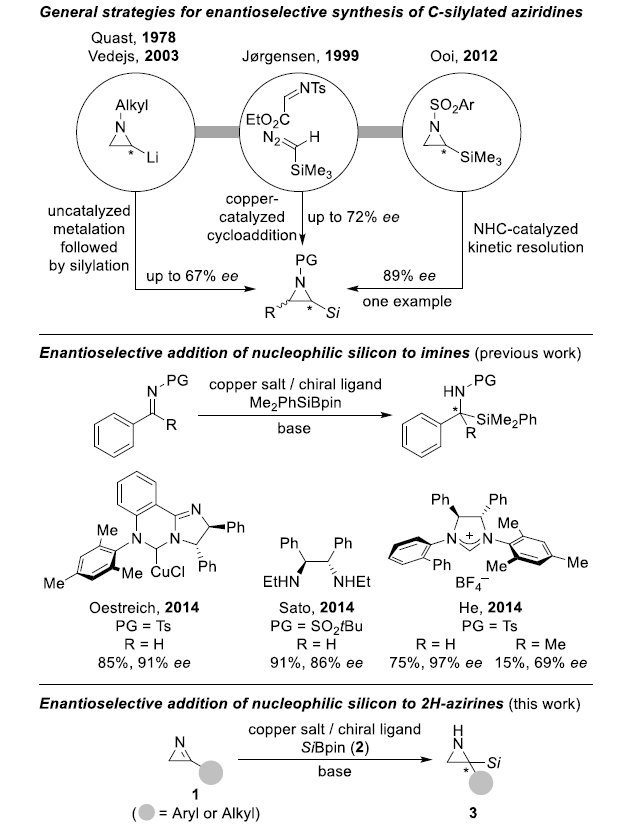
图1. 研究背景(图片来源:Angew. Chem. Int. Ed.)
首先,作者以1a为模型底物进行了底物筛选。最终发现当反应体系组成为Cu(CH3CN)4PF6(3.0 mol%)、(R,R)-Ph-BPE (L1, 3.6 mol%)、LiOtBu(40 mol%)、Me2PhSiBPin(2a,1.5当量)、MeOH:H2O(1:1,2.0当量)和THF作溶剂时可以98%产率和95% ee得到目标产物(S)-3aa。

图2. 条件筛选(图片来源:Angew. Chem. Int. Ed.)
随后,作者在最优条件下进行了底物拓展。含烷基取代芳基的2H-吖丙因1b-f的反应结果与1a相似。1h中的联苯取代基和1i中的萘取代基与反应完全兼容。1j-m中的甲氧基和苄氧基以及1n中受保护的邻苯二酚对产率和对映选择性均无影响;1o中的硫醚同样可以耐受。同样,1p中的乙酰氧基和1q中的三氟甲氧基对结果也没有影响。像三氟甲基(1r)、氰基(1s)和乙酰基(1t)等强吸电子基团也可反应,但效果较差。卤代底物1u-z得到的产物同样产率高,对映选择性好。具有一个邻位取代基的二卤代衍生物1a'和1b'随着卤素基团大小的增加,对映性选择性有降低的趋势(F在3a'a中时ee为86%, Cl在3b'a中时ee为50%)。对于杂环来说,1c'的噻吩环的对应产物3c'a的ee值相比之下较低,为77%。一些3-烷基取代的2H-吖丙因(灰色框)表明,2°烷基取代基 (3d'a为80% ee)对映体选择性略有减弱,但1°烷基取代基仍然效果较好。通过X-射线衍射数据,作者确证了3na和3pa的绝对构型为S。总的来说,该反应具有极好的官能团耐受性。
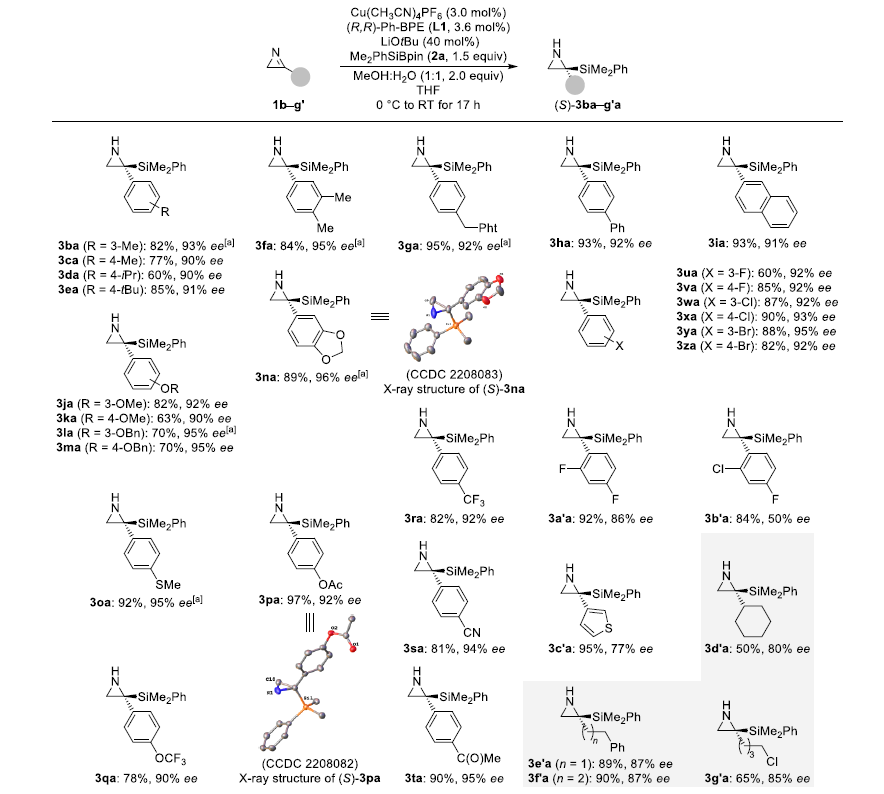
图3. 底物拓展一(图片来源:Angew. Chem. Int. Ed.)
为了确定该方法是否适用于其它亚胺,作者又尝试了张力较小的环酮亚胺4以及非环N-甲基取代的醛亚胺5和酮亚胺6,它们都没有得到预期的结果。这强调了在2H-吖丙因中高活性C=N键的必要性。作者还用1a与其它Si-B试剂2b-d进行反应,但只有与Et3SiBpin (2b)的反应以84%的产率和64%的ee得到产物。具有较大硅基的硅基硼酯2c和2d不参与加成反应,起始原料也没有转化。
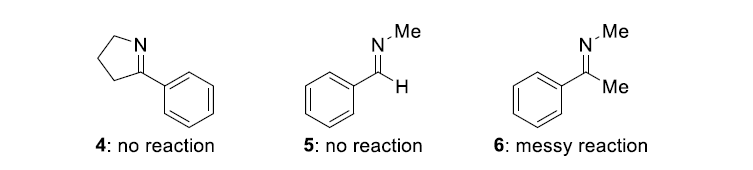
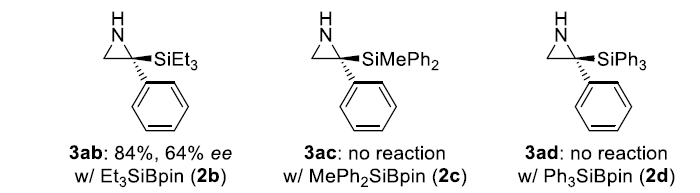
图4. 底物拓展二(图片来源:Angew. Chem. Int. Ed.)
为了展示这一反应的应用价值,作者对(S)-3aa进行了两次转化。未保护的(S)-3aa用3,5-二硝基苯甲酰氯酰化,然后用Lawesson试剂处理,这一过程将经历酰胺的重排以产生构型保留的噁唑啉衍生物(S)-7。此外,磺胺(S)-8氢化得到β-硅胺衍生物(S)-9,收率为95%,ee为90%。
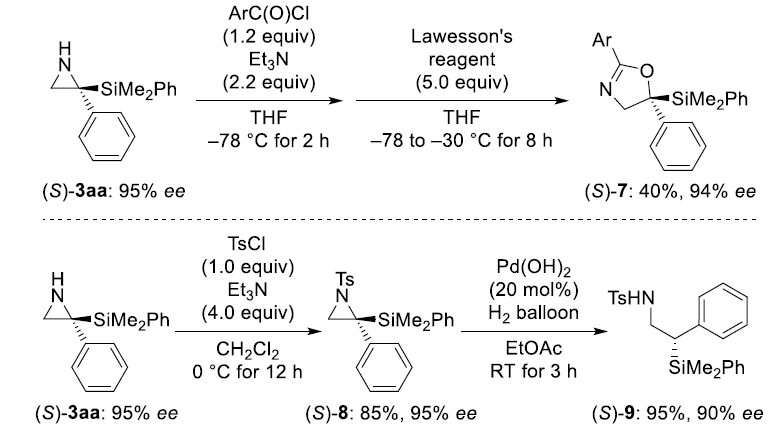
图5. 反应应用(图片来源:Angew. Chem. Int. Ed.)
为了解释该反应对映选择性的成因,作者基于建立的铜(I)-(R,R)-Ph-BPE手性络合物模型,提出了两种可能的过渡态。如图6所示,手性催化剂口袋的一个空缺部分可以容纳2H-吖丙因C3上的取代基(左),而另一个过渡态因为该取代基与配体骨架上的苯基之间的空间相互作用导致斥力较大,从而导致该过渡态不利于反应进行(右)。这与绝对构型是S的结果是一致的。该模型还有助于理解为什么体积较大的硅基没有迁移,这是因为对于三乙基硅基来说,由于没有π-π堆叠相互作用,过渡态并不紧凑不足以发生这一过程。
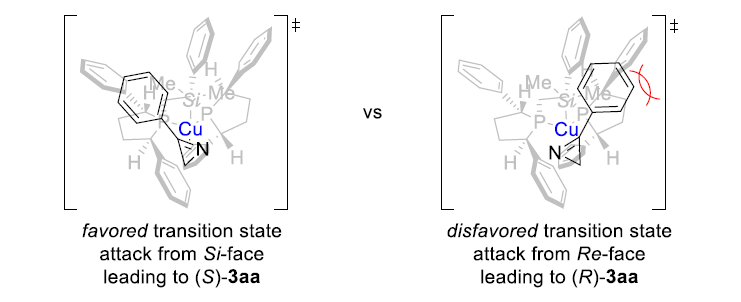
图6. 反应过渡态(图片来源:Angew. Chem. Int. Ed.)
总结
Martin Oestreich课题组首次报道了C-硅基化,N-未保护的氮杂环丙烷的催化不对称合成。这是通过对映选择性铜催化3-取代的2H-吖丙因与硅基硼酯的加成反应实现的。与其它环酮亚胺和非环酮亚胺相比,这些较大张力的环酮亚胺具有足够的反应性,即亲电性,可以实现预期的目标。该反应具有极好的官能团耐受性,具备一定应用价值。
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn