- 首页
- 资讯
ACS Chem. Biol.:苏州大学史海斌教授课题组发现线粒体共价锚定提高肿瘤放射敏感性的新机制
来源:苏州大学放射医学与辐射防护国家重点实验室 2022-07-20
导读:近日,苏州大学放射医学与辐射防护国家重点实验室史海斌教授课题组在肿瘤放射增敏治疗研究方面取得新进展,相关成果以“Endogenous ROS-mediated Covalent Immobilization of Gold Nano-particles in Mitochondria: A “Sharp Sword” in Tumor Radiotherapy”为题在线发表在国际知名杂志ACS Chemical Biology上( Doi:10.1021/acschembio.2c00475)。
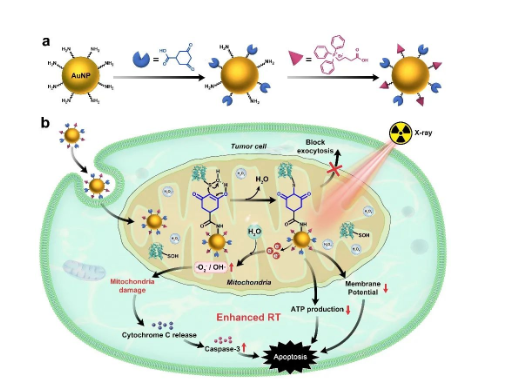
金纳米颗粒是一种极具应用潜力的放疗增敏剂,小尺寸金纳米颗粒由于具有强的肿瘤渗透能力和较长的血循环周期,更加适用于活体肿瘤的成像与治疗研究。然而由于其粒径过小,则会被组织器官快速代谢排出体外,无法在肿瘤病灶区长时间富集,导致放射治疗效果不佳的问题。因此,研发能使小尺寸纳米金高富集长滞留于肿瘤病灶组织的新技术,对于提高活体肿瘤的放射治疗效果意义重大。此外,由于纳米颗粒受到X射线照射后产生的次级电子的射程较短,仅有几十纳米,亚细胞靶向近年来成为开发高效放射敏化剂的新方向。线粒体作为真核细胞中起供能作用的细胞器,细胞中约90%的活性氧(ROS)产生于此,大量研究证明,ROS失衡会破坏线粒体膜,导致凋亡因子细胞色素c的释放,从而引发细胞死亡。因此,线粒体是提高肿瘤放射治疗的重要靶点。在最新的研究进展中,史海斌教授课题组策略性将1,3-环己二酮和线粒体靶向基团三苯基膦(TPP)修饰于金纳米颗粒表面,制备获得一种线粒体靶向且特异性与次磺酸化蛋白发生共价键反应的新型纳米金dAuNP-TPP。由于肿瘤细胞的线粒体里存在高浓度ROS及高表达次磺酸化蛋白,当dAuNP-TPP靶向并蓄积于肿瘤细胞的线粒体后,会与次磺酸化蛋白发生共价交联反应,长时间滞留于肿瘤,实现活体肿瘤的高灵敏CT成像及放射增敏治疗。更重要的是,我们还意外发现纳米金与肿瘤细胞线粒体内的次磺酸化蛋白发生共价交联反应后,会诱发线粒体的膜电势和ATP水平均显著降低,线粒体的完整性受到严重破坏,导致细胞凋亡发生,进一步提高了肿瘤细胞的放射治疗敏感性,为实现肿瘤的高灵敏诊断与高效治疗提供了新思路。本论文第一作者为苏州大学2019级硕士研究生赵燕,放射医学与辐射防护国家重点实验室史海斌教授为本论文的通讯作者,苏州大学为该论文第一单位。该工作得到国家自然科学基金重大研究计划、国家自然科学基金面上项目、江苏省重点研发计划及江苏省放射医学与防护重点实验室开放课题等项目的共同资助。论文链接:https://pubs.acs.org/doi/full/10.1021/acschembio.2c00475。 参考资料:http://sklrmp.suda.edu.cn/af/f6/c8750a503798/page.psp
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn