

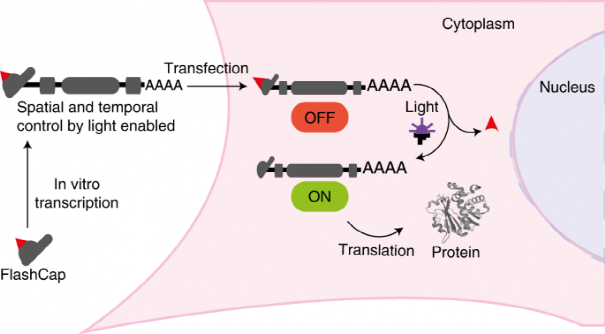
图1. 光笼5'帽类似物用于光控mRNA翻译示意图(图片来源:Nat. Chem.)
研究背景
信使RNA(简称mRNA)是一种参与蛋白质合成的单链RNA。mRNA的作用是将蛋白质信息从细胞核中的DNA传送到细胞质,随后读取mRNA序列并将每个三碱基密码子翻译成其相应的氨基酸。真核生物mRNA具有特定的 5'帽结构,其通过5'-5'三磷酸桥将N7-甲基化鸟苷连接到第一个转录核苷酸。5'帽结构在翻译起始中起关键作用,主要归因于 N7 甲基化鸟苷对于翻译起始因子eIF4E的特定识别。同时5'帽对于许多mRNA质控起关键作用,并保护真核mRNA免受外切酶降解。mRNA周转和体内平衡需要专用的去盖酶(Dcp1-2、DcpS)。5'帽与3'末端的poly(A)尾一起形成mRNA“闭环”,从而促进eIF4E和poly(A)结合蛋白之间的相互作用。没有5'帽的RNA几乎不翻译,并且具有高度免疫原性。因此,用于生物学研究和治疗应用的mRNA的生产通常涉及5'-加帽。
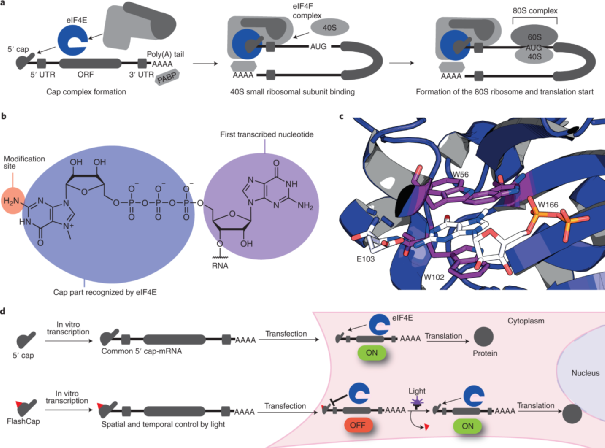
图2. 真核生物mRNA翻译启动过程以及化学修饰的位点(图片来源:Nat. Chem.)
关键合成步骤
作者通过在5'端鸟苷N2引入光裂解基团,其中氨基甲酸甲酯作为桥连物可在光作用下有效裂解。以鸟苷为起始反应物,首先使用三甲基甲硅烷基氯化物(Me3SiCl)保护羟基。然后在一锅反应中,将鸟苷的游离氨基转化为异氰酸酯,通过与邻硝基苄基 (ONB) 醇、3,4-二甲氧基- 2-硝基苄基(DMNB)醇、6-硝基胡椒基(NP)醇、6-硝基胡椒基-甲基(NPM)醇反应,形成光可裂解基团或红移衍生物。之后用氨水(THF溶液)去除TMS基团以获得光笼鸟苷。然后将光笼鸟苷在5'-OH处单磷酸化以产生图二中6a,b化合物,甲基化后形成化合物7a,b,并与鸟苷-5'-二磷酸咪唑啉偶联从而得到最终产物。
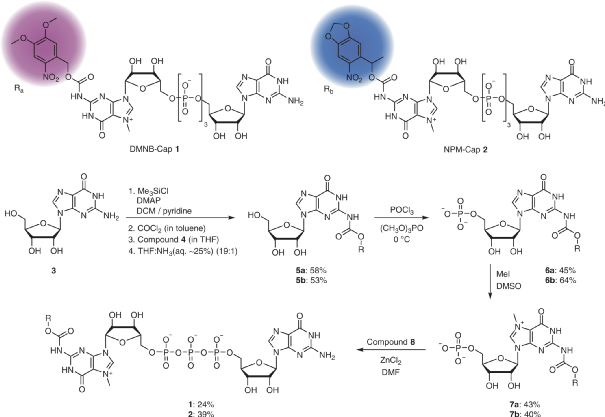
图3. 具有光可裂解基团(FlashCaps)的帽类似物以及光触发翻译的整体合成思路(图片来源:Nat. Chem.)
结构及性能分析
作者进一步分析了N2位置具有光可裂解基团鸟苷的吸收光谱。ONB鸟苷仅在300 nm以上显示低吸光度,DMNB鸟苷在350 nm处显示最大吸收,NP和NPM鸟苷略微红移,在360 nm处达到最大值。为了选择最适合生物应用的光可裂解基团,作者在中性pH的水溶液中照射并分析它们的减少以及天然鸟苷的形成的HPLC和LC-MS谱图。结果表明,在365 nm处,短时间照射(5-15 s)足以去除10 μL 500 μM 溶液中的光裂解基团,释放游离鸟苷。在 405 nm,NP、NPM和DMNB组在60 s后被有效去除,比ONB组更有效。在420 nm,NPM组在120 s后完全去除。因此,作者最终选择了DMNB和NPM组进行进一步研究,并合成了各自的cap0类似物。生成的FlashCaps在N2位置包含DMNB或NPM基团。它们在300 nm以上的吸收光谱和它们的解笼罩动力学类似于各自的光笼鸟苷。其还还通过在细胞裂解物中孵育cap 0或FlashCaps,然后进行HPLC分析来评估氨基甲酸酯键的生物稳定性。FlashCaps在30小时内表现出高稳定性,表明氨基甲酸酯键不是裂解液降解的主要点。
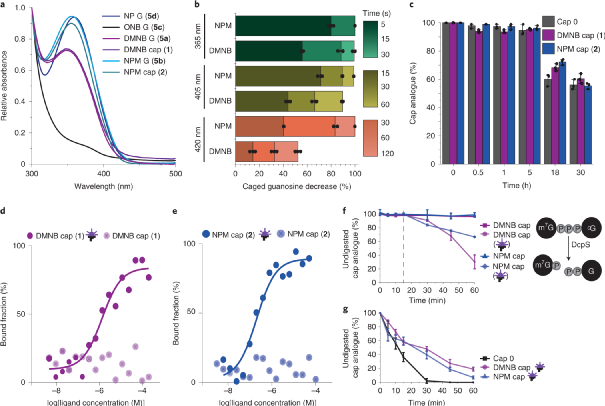
图4. 光可裂解基团 (FlashCaps)基本表征(图片来源:Nat. Chem.)
随后,作者评估了光可裂解基团如何影响5'帽与eIF4E的相互作用。在光笼帽存在的情况下,使用微量热泳(MST)对FlashCaps和Cy5标记的eIF4E的结合测量发现没有产生结合曲线。在相同条件下,光诱导去除光笼基后,则获得了与帽0相似范围内的特征结合曲线和Kd值(0.3 μM),表明帽0有效形成。作者同时还研究了光可裂解基团如何影响与帽修饰酶的相互作用。DcpS是一种焦磷酸酶,可在真核细胞中将帽结构水解为m7GMP和GDP。结果表明,与eIF4E的结果相似,DcpS——一种结合但非切割的脱帽酶变体——与cap0相互作用,但不与FlashCaps相互作用。
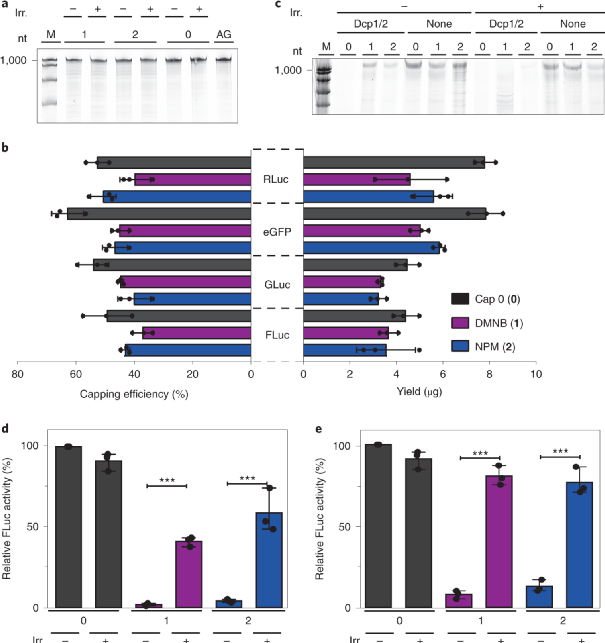
图5. 光可裂解基团 (FlashCaps)修饰的mRNA基本表征(图片来源:Nat. Chem.)
总结
随着新冠的大爆发,信使RNA(mRNA)新冠疫苗再次成为研究热点,其中以Moderna和BioNTech/Pfizer为代表,它们编码刺突蛋白可有效防止SARS-CoV-2感染。mRNA技术不仅限于疫苗接种,还可改善自身免疫性疾病以及实现个性化的癌症治疗。然而,到目前为止,还没有策略可以有效实现定时、定点mRNA表达,即在不改变mRNA性能的前提下控制特定组织的递送和摄取。在本文中,研究人员开发了一种通过光控制mRNA翻译的技术——FlashCaps。FlashCaps作为mRNA5'帽类似物,通过裂解氨基甲酸酯键连接的单个光笼基基团,导致快速有效地释放天然结构。FlashCap-mRNAs具有以下优势:(1)仅包含一个光可切割基团;(2)无光照时可暂停蛋白质翻译;(3)定时、定点释放天然 cap 0(无帽结构)-mRNA;(4)不改变mRNA自身序列;(5)不具有免疫原性。

图6. Andrea Rentmeister 教授(图片来源:Muenster university)
Andrea Rentmeister教授在格拉茨大学和波恩大学获得化学工程和化学专业博士学位,之后加入加州理工学院弗朗西斯·阿诺德实验室(2018年诺贝尔奖获得者)进行博士后研究。2010年成为汉堡大学生物化学初级教授。目前,她在明斯特大学担任生物分子标记化学教授。致力于了解mRNA翻译机制并最终控制其特定转录及翻译。开发多种化学和化学酶促方法,对mRNA进行分子水平上操作、分析以及控制,并将其应用于活细胞以及体内。

图7. Andrea代表奥地利参加2000年夏季奥运会参赛照片(图片来源:Imago)
文章详情:
Klöcker, N., Weissenboeck, F.P., van Dülmen, M. et al. Photocaged 5′ cap analogues for optical control of mRNA translation in cells. Nat. Chem. (2022). https://doi.org/10.1038/s41557-022-00972-7
课题组网页:https://www.uni-muenster.de/Cells-in-Motion/people/all/rentmeister-a.php

长按或扫码左侧二维码查看原文
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn