

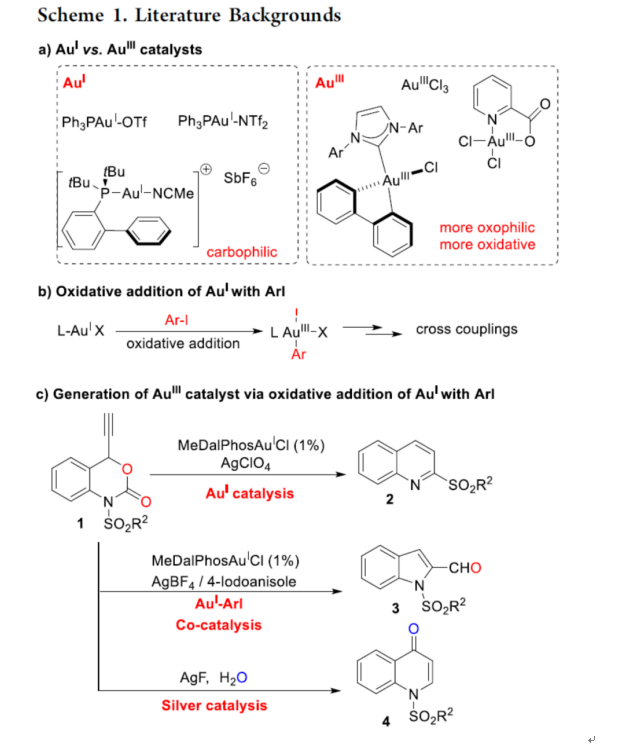
阳离子金催化剂是活化不饱和C-C键最为有效的催化剂之一,如常见的AuI和AuIII配合物(Scheme 1a)。AuI催化剂是线性的双配位配合物,通常更具亲碳性。另一方面,AuIII配合物具有四配位平面几何构型,通常更具亲氧和亲电性。因此,AuI和AuIII催化剂通常表现出独特的反应性和选择性。如,在Toste课题组报道的α,β-不饱和醛与乙烯酮硅基缩醛的Mukaiyama-Michael反应中,通过使用AuI和AuIII催化剂,从而使反应具有发散性。
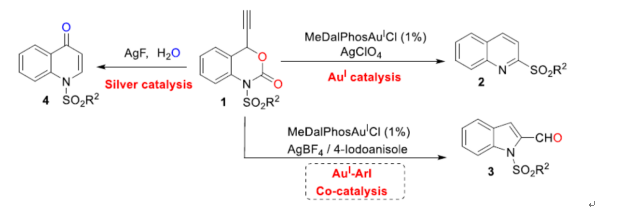
虽然AuIII配合物(如AuCl3、NaAuCl4等)经常用于金催化的开创性研究中,但AuIII配合物通常具有高氧化性,并且易于分解或导致反应的复杂性。因此,与AuI催化剂相比,对于AuIII催化剂的开发与研究极具挑战。其中,AuI催化剂的氧化加成是合成AuIII催化剂的一种有效方法,但强氧化剂的使用导致官能团耐受性差。最近,Bourissou课题组报道了一种通过使用半稳定配体用于引发ArI与AuI催化剂的氧化加成反应(Scheme 1b)。在此,东华大学胥波课题组报道了一种AuI-催化、AuI-ArI共催化和银催化乙炔基苯并噁嗪酮的发散性策略,从而分别合成了一系列磺酰基喹啉、甲酰基吲哚和喹诺酮衍生物(Scheme 1c)。
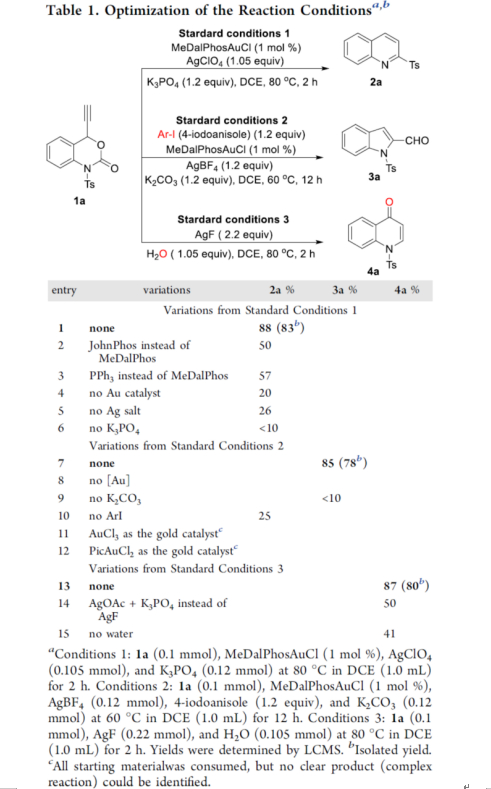
首先,作者以乙炔基苯并噁嗪酮1a作为模型底物,进行了相关反应条件的筛选(Table 1)。当以MeDalPhosAuCl作为催化剂,AgClO4作为银盐,K3PO4作为碱,在DCE溶剂中反应,能以88%的收率获得磺酰喹啉产物2a。其次,当以MeDalPhosAuCl作为催化剂,ArI作为共催化剂,AgClO4作为银盐,K2CO3作为碱,在DCE溶剂中反应,可以85%的收率得到吲哚产物3a。此外,当以AgF作为催化剂,水作为添加剂,在DCE溶剂中反应,可以87%的收率得到喹诺酮产物4a。
(图片来源:ACS Catal.)
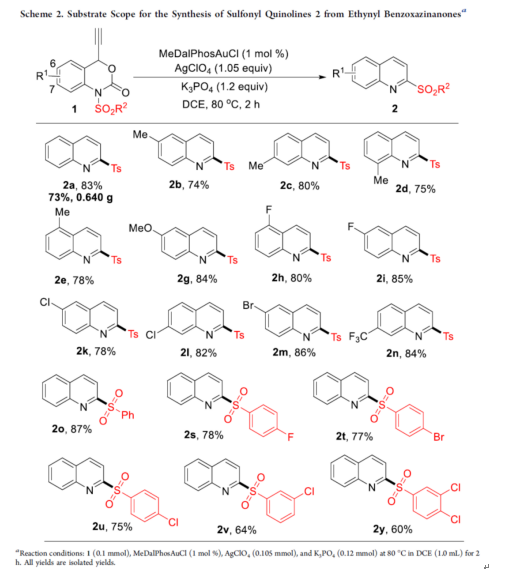
在获得上述最佳反应条件后,作者首先对合成磺酰基喹啉的底物范围进行了扩展(Scheme 2)。首先,当底物1中的R1为-Me、-OMe、-F、-Cl、-Br、-CF3时,均可顺利反应,获得相应的磺酰基喹啉产物2b-2n,收率为74-86%。其次,当底物1中的R2为苯基、卤素取代的苯基时,也与体系兼容,获得相应的磺酰基喹啉产物2o-2y,收率为60-87%。此外,克级规模实验,可以73%的收率获得磺酰基喹啉产物2a。
(图片来源:ACS Catal.)
紧接着,作者对合成甲酰基吲哚的底物范围进行了扩展(Scheme 3)。首先,当底物1中的R1为-Me、-OMe、-F、-Cl时,均可顺利反应,获得相应的甲酰基吲哚产物3b-3l,收率为65-83%。其次,当底物1中的R2为苯基、取代的苯基、萘基时,也与体系兼容,获得相应的甲酰基吲哚产物3o-3v,收率为60-75%。此外,克级规模实验,也可以68%的收率得到甲酰基吲哚产物3a。
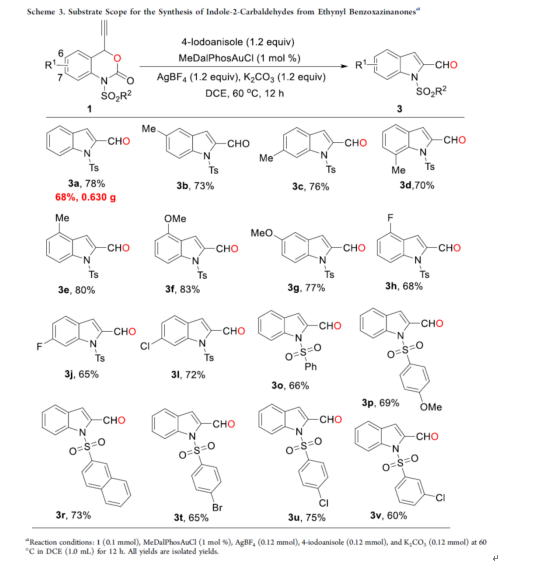
(图片来源:ACS Catal.)
随后,作者对合成喹诺酮的底物范围进行了扩展(Scheme 4)。首先,当底物1中的R1为-Me、-OMe、-F、-Cl、-Br、-CF3时,均可顺利反应,获得相应的喹诺酮产物4b-4n,收率为73-83%。其次,当底物1中的R2为苯基、不同电性取代的苯基、萘基时,也与体系兼容,获得相应的喹诺酮产物4o-4y,收率为63-84%。此外,克级规模实验,也可以71%的收率得到喹诺酮产物4a。
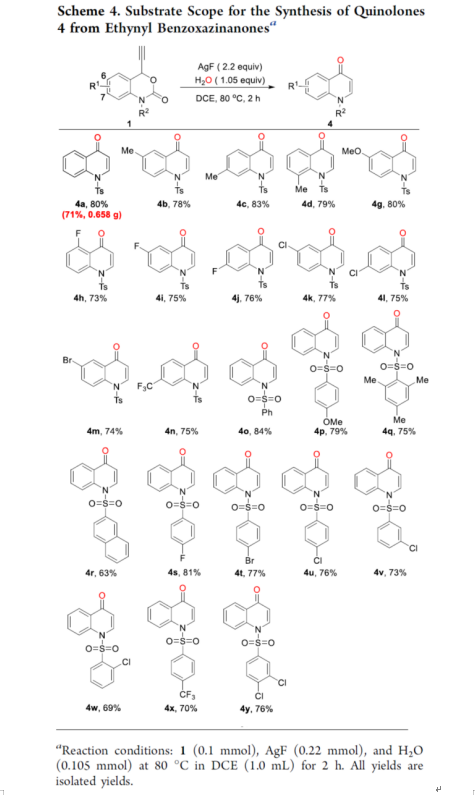
(图片来源:ACS Catal.)
为了进一步了解反应的机理,作者进行了相关的控制实验(Scheme 5)。首先,通过18O-标记实验表明,水不是吲哚-2-甲醛3a中的氧来源(Scheme 5a),水是喹诺酮4a中的氧来源(Scheme 5b)。同时,1x在三种标准条件下,均未能生成相应的目标产物,从而说明末端炔烃的重要性(Scheme 5c)。其次,通过文献预合成的Ar-AuIII-I,同样具有相似的催化效率(Scheme 5d)。此外,与经典的AuI-催化体系相比,AuI-ArI共催化体系具有独特的选择性,如炔酮与磺胺类加成反应(Schemes 5e-5f)、2-(炔醇)芳基醛或酮环化反应(Schemes 5g-5h)、苯并噁唑与炔酰胺的环化反应(Schemes 5i-5j)。
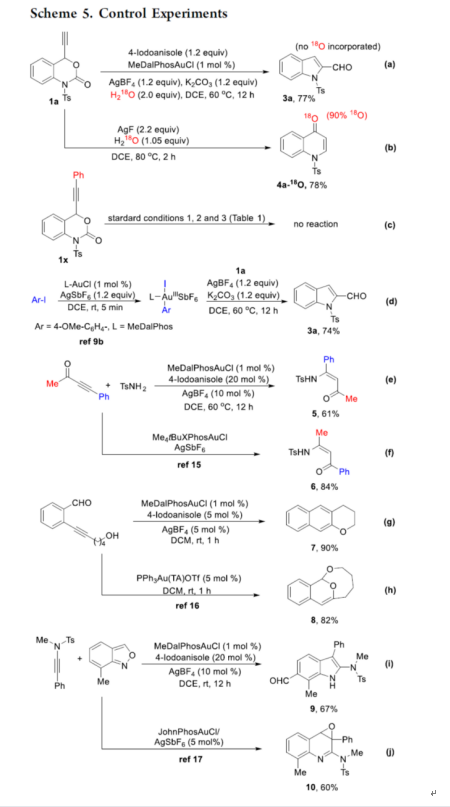
(图片来源:ACS Catal.)
最后,作者提出了三种合理的催化循环过程(Scheme 6)。在AuI-催化体系中(Scheme 6a),首先,1a经6-endo-dig环化生成中间体A,A中的磺酰基迁移后形成碳阳离子中间体B。B中的磺酰基迁移可生成中间体C。或者,A可直接转化为中间体C(金(I)卡宾)。其次,C经阳离子金的1,2-H迁移和断裂,生成中间体D。D经碱介导的去羰基化后,生成中间体G。最后,H经碱介导的脱水过程,可生成喹啉产物2a。在AuI-ArI共催化体系中(Scheme 6b),AuI与Ar-I经氧化加成原位生成Ar-AuIII-I。1a经5-exo-dig环化生成中间体I。I经碱介导去羰基化后,生成中间体K。K可能经Au(I)-介导的1,3-烯丙醇异构化,生成中间体L。L经进一步的氧化后,可获得吲哚产物3a。在Ag-催化体系中(Scheme 6c),1a经银介导6-endo-dig环化生成中间体N。其次,N经碱介导的去羰基化后,生成醇中间体P。最后,P经氧化可生成喹诺酮产物4a。初步理论研究表明,发散性的起源(5-exo-dig vs 6-endo-dig)并非第一个环化步骤。
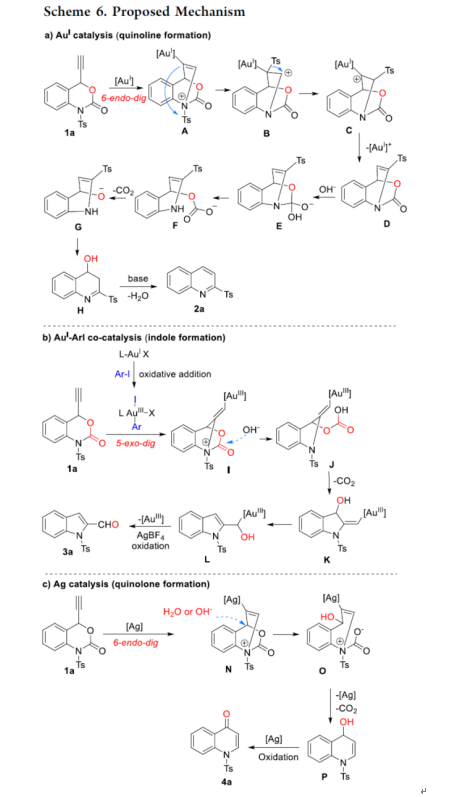
(图片来源:ACS Catal.)
总结:东华大学胥波课题组报道了一种AuI-催化、AuI-ArI共催化和银催化乙炔基苯并噁嗪酮的发散性策略,从而分别合成了一系列磺酰基喹啉、甲酰基吲哚和喹诺酮衍生物。同时,该反应具有底物范围广泛、官能团兼容性高、化学与区域选择性出色等特点。
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn