

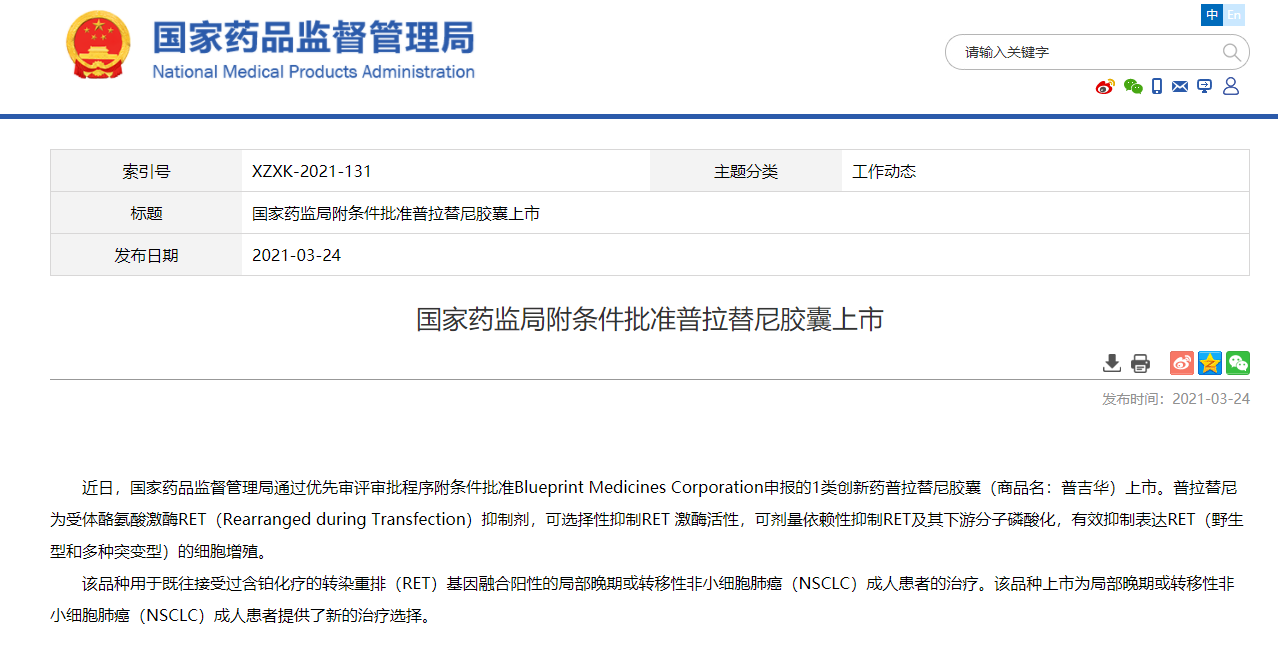
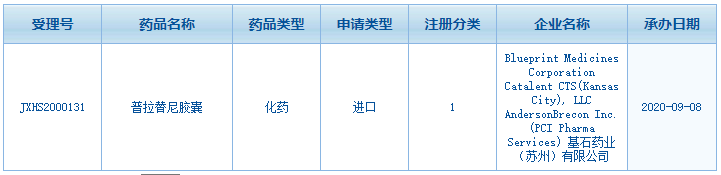
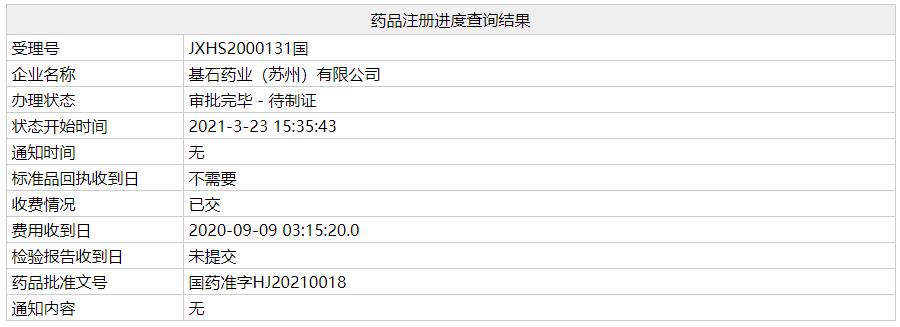
基石药业(香港联交所代码:2616),一家专注于开发及商业化创新肿瘤免疫疗法及精准治疗药物的领先生物制药公司,今日宣布,中国国家药品监督管理局(NMPA)批准普吉华®(普拉替尼胶囊)作为国家一类新药上市申请,用于既往接受过含铂化疗的转染重排(RET)基因融合阳性的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者的治疗。这标志着中国第一个选择性RET抑制剂的获批上市,同时基石药业也迎来了首个商业化上市的产品。
基石药业董事长兼首席执行官江宁军博士表示:“这是一个历史性的重要时刻。普吉华®的获批印证了基石药业立足解决患者未满足的临床痛点与诉求的决心,并体现了基石药业将创新药物快速推向市场的能力。我们感谢所有为普吉华®的临床开发做出贡献的患者和研究者们,以及国家药监局为普吉华®的获批而开展的优先审评审批工作,同时也非常感谢各级政府给予的支持。我们将继续全力推进普吉华®在中国的研发,更广泛地评估其在包括一线NSCLC、甲状腺癌和其它实体瘤患者中的疗效,尽快惠及更多患者。”
ARROW研究主要研究者、广东省人民医院吴一龙教授表示:“在肺癌精准治疗领域,RET靶点的研发是一个巨大的突破。ARROW研究的优异数据结果有力支持了此次普吉华®在中国获批,并有望改变国内RET融合阳性非小细胞肺癌患者的治疗标准。”
ARROW研究是一项旨在评估普拉替尼在RET融合阳性NSCLC、RET突变型甲状腺髓样癌和其他RET融合的晚期实体瘤患者中的安全性、耐受性和有效性的全球临床研究。研究数据显示,普拉替尼在经含铂化疗的RET融合阳性的NSCLC中国患者中显示出了优越和持久的抗肿瘤活性,总体缓解率(ORR) 为56%,中位缓解持续时间(DOR)未达到,6个月的DOR率为83%,安全性及耐受性良好,未出现与普拉替尼相关的不良事件导致的终止治疗或死亡。
普拉替尼是一种强效、选择性RET抑制剂,由基石药业合作伙伴Blueprint Medicines公司开发。基石药业与Blueprint Medicines公司达成了独家合作和许可协议,获得普拉替尼在大中华地区,包括中国大陆、香港、澳门和台湾地区的独家开发和商业化权利。
关于RET融合阳性非小细胞肺癌
近年来肺癌发病率在中国持续增长。中国在2018 年约有77万新增肺癌病例。同样在2018 年,中国约有69万肺癌导致的死亡病例。在男性和女性癌症患者中,肺癌均为癌症相关死亡的主要原因。其中,非小细胞肺癌占肺癌的大多数。
在肺癌领域,EGFR、ALK、ROS1等驱动基因突变已广泛普及,针对这些驱动基因的靶向药物均已获批上市。RET融合是新近发现的肺癌驱动基因,在非小细胞肺癌中RET融合患者约占1- 2%,常见于不吸烟的年轻人群。
关于普吉华®(普拉替尼胶囊)
普吉华®是一种口服、每日一次、强效高选择性RET抑制剂,已获中国国家药品监督管理局批准,用于治疗既往接受过含铂化疗的转染重排(RET)基因融合阳性的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者。
美国食品药品监督管理局(FDA)批准其以商品名为GAVRETO™上市销售,分别用于治疗经FDA批准的检测方法检测证实为转移性RET融合阳性NSCLC的成人患者、需要系统性治疗的晚期或转移性RET突变甲状腺髓样癌成人和12岁及以上儿童患者,以及需要系统性治疗且放射性碘难治(如适用)的晚期或转移性RET融合阳性甲状腺癌成人和12岁及以上儿童患者。
普拉替尼在中国、美国还未获批用于其他适应症,或者其他地区的医疗监管机构均未对普拉替尼的任何适应症做出批准决定。
普拉替尼旨在选择性地和有效地靶向致癌性RET突变,包括可能导致治疗耐药的继发性RET突变。在临床前研究中,普拉替尼抑制RET的浓度低于其他药物相关激酶,包括VEGFR2、FGFR2和JAK2。
全球范围内,针对普拉替尼用于治疗RET融合阳性的NSCLC、各类甲状腺癌以及其他实体瘤患者的临床开发正在进行。欧洲药品管理局受理了普拉替尼的上市许可申请,用于治疗RET融合阳性NSCLC。FDA授予普拉替尼突破性疗法认定,用于治疗铂类化疗后进展的RET融合阳性NSCLC,以及需要全身治疗且尚无替代疗法的RET突变阳性甲状腺髓样癌。
关于基石药业
基石药业(HKEX: 2616)是一家生物制药公司,专注于开发及商业化创新肿瘤免疫治疗及精准治疗药物,以满足中国和全球癌症患者的殷切医疗需求。成立于2015年底,基石药业已集结了一支在新药研发、临床研究以及商业运营方面拥有丰富经验的世界级管理团队。公司以肿瘤免疫治疗联合疗法为核心,建立了一条14种肿瘤候选药物组成的丰富产品管线。目前,已有1款药物在中国大陆获批上市。多款后期候选药物正处于关键性临床试验或注册阶段。基石药业的愿景是成为享誉全球的生物制药公司,引领攻克癌症之路。
前瞻性声明
本文所作出的前瞻性陈述仅与本文作出该陈述当日的事件或资料有关。除法律规定外,于作出前瞻性陈述当日之后,无论是否出现新资料、未来事件或其他情况,我们并无责任更新或公开修改任何前瞻性陈述及预料之外的事件。请细阅本文,并理解我们的实际未来业绩或表现可能与预期有重大差异。本文内所有陈述乃本文章刊发日期作出,可能因未来发展而出现变动。
商标
Blueprint Medicines, GAVRETO及其相关商标为Blueprint Medicines Corporation所有。
参考资料
[1] 美通社,基石药业宣布中国首个选择性RET抑制剂普吉华(R)(普拉替尼胶囊)获批 为肺癌患者提供治疗新选择,https://www.prnasia.com/story/312515-1.shtml
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn