

一、生物技术药物发展现状
1.生物技术药物产业和市场
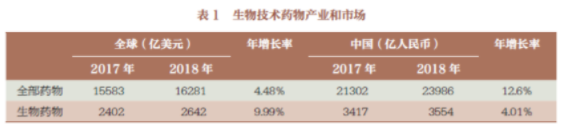
生物技术药物发展现状与整体医药技术的发展相关。回顾2018 年的市场情况,全球医药市场规模是16281 亿美元,比2017 年同比增长了4.48%。中国的医药市场规模是23986 亿人民币,占全世界市场的21%。我们的医药市场增长幅度还是比较快的,年增长率为12.6%。但是我们在生物技术药物方面增长比较慢一些,全世界市场是2642 亿美元,年增长率是9.99%,中国生物技术药物市场是3554 亿人民币,占全球的19%。2018 年生物技术药物市场的年增长率是比较低的,只有4.01%(表1)。
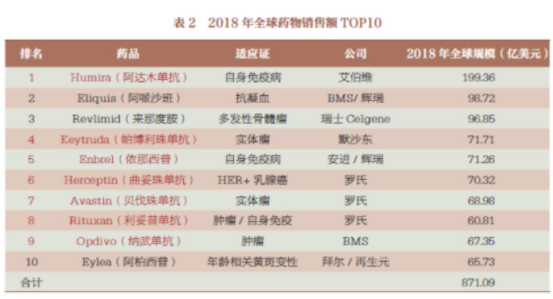
2. 2018 年全球药物销售TOP10
2018 年全球销售最好的10 个药物,其中有7 个是抗体药物(表2 中颜色标示),阿达木单抗的靶点是Tnfα,它的销售到了199 亿美元,这对于单药销售来说是很大的数量。PD-1 的抗体药物,包括依那西普以及曲妥珠单抗、贝伐珠单抗、利妥昔单抗,这都是过去传统的产品,还有纳武单抗、帕博利珠单抗,都挤入了TOP10。最后两个抗体药物上市时间并不是很长,但是很快进入了前10。所以整个全球药物销售,从表2 可以看到,生物技术药物尤其是抗体药物的市场占了很大的比重,大概是在2000 多亿美元药物市场中占了1650 亿美元,占比62.5%。
二、癌症发病情况和肿瘤治疗
中国抗肿瘤药物占生物药物比例比较高,约24.6%。新时代的免疫治疗药物,从过去的三分天下——抗体药物、疫苗与细胞治疗、基因治疗的药物,到现在抗体药物已经占全部生物药物76%,其中抗肿瘤药物36 个。因此,肿瘤免疫治疗是非常重要的。
1.癌症发病情况
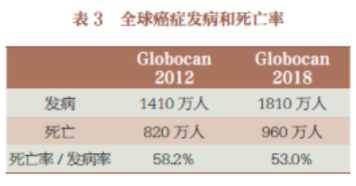
全球癌症的发病率居高不下,一个重要的原因是人口的增长和平均寿命的增加。全球目前约有70 亿人,据最近的一次人口普查统计,中国人口是13.95 亿。中国的老龄人口目前占比12%。我们的平均寿命较以往有所增加,目前是76.4 岁,在全球的第50 位,日本是世界第一,86.2 岁,比我们差不多高10 岁。日本的老龄化程度比较严重,他们65 岁以上的老龄人口占28%,这是相当大的一个比例。老年人口的增加和癌症发病率有关,全球2018 年癌症发病人数是1810 多万,死亡人数是960 万。全球癌症死亡人数有所增加,主要由于人口老龄化,还有危险因素的持续存在,包括食品、环境的污染。但是我们也要看到,2012 年的时候癌症死亡率/ 发病率是58.2%,到2018 年下降到53%。虽然发病人数和死亡人数没有降低,但是死亡率/ 发病率的比例降低了,表明癌症治疗有长足的进步(表3)。
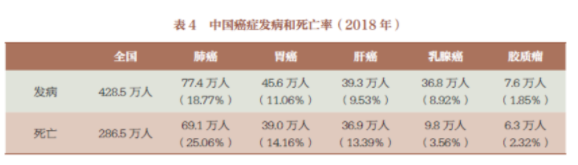
在中国,癌症的发病是428.5 万人,死亡是286.5 万人(表4),约占全球发病和死亡人数的25%。世界卫生组织关注中国发病率、死亡率居前四位的癌症是肺癌、胃癌、肝癌和乳腺癌。和2016 年相比,2018 年乳腺癌发病人数上升。欧美国家乳腺癌发病率一直比较高,原来中国乳腺癌发病率比较低,可是到了2018 年乳腺癌上升成为中国的第四大癌症,值得重视的是乳腺癌要早诊早治。
还有一个发病趋势是脑胶质瘤的增加。脑胶质瘤从发现到死亡,平均生存时间只有一年多,而且特别容易复发,发病率与死亡率很接近,发病是7.6万人,死亡是6.3 万人(表4)。
2. 肿瘤治疗发展历程
肿瘤治疗发展历程经过了三次革命,最早是1942 年美国耶鲁大学发现了芥子气的衍生物氮芥治疗淋巴瘤,开创了肿瘤化学治疗药物的先河。后来逐渐发现化疗药物毒副作用比较大,既杀伤肿瘤细胞,也杀伤正常细胞。直到2003 年发现了一个重要的药物,叫吉非替尼(易瑞沙),这个药物是针对TGFR TK 激酶的靶向药物。靶向药物的发现大大降低了药物的毒副作用。但是好景不长,很快有一部分病例产生了耐药。2010 年美国FDA批准了第一个DC 疫苗——Provenge,用于治疗前列腺癌,推动了免疫治疗的发展。业内公认2010 年是免疫治疗的1.0 版本。
2017 年8 月30 日,美国FDA 紧急批准了诺华抗急性淋巴细胞白血病的CD19CAR-T 药物Kymriah 上市;同年10 月18 日,FDA 批准了Kate Pharma 的CD19CAR-T 药物Yescarta上市,用于治疗成人大B 淋巴细胞瘤。由于这两个CAR-T 药物的紧急上市,进一步推动了免疫治疗的发展。2017 年美国临床肿瘤学会年会(ASCO)上称目前已经进入群雄逐鹿的肿瘤免疫治疗2.0 版本时代。所以,对于肿瘤治疗的发展,在手术治疗、放疗、化疗之后,免疫治疗已经成为第四大肿瘤治疗技术,免疫治疗也可以成为一线药物,这是一大进步。
三、现代免疫治疗
抗体等大分子药物及免疫治疗,是近年生物药物领域发展的生力军,目前包括5 大类药物,分别是:①单克隆抗体药物(如美罗华、赫赛汀);②抗免疫检查点抗体药物(如PD-1,CTLA-4);③免疫T 细胞治疗,包括过继性T 细胞治疗(ACT)、肿瘤浸润淋巴细胞(Expanded TILS)、基因工程T 细胞(CAR-T,TCR-T);④ 树突状细胞疫苗(DCs vaccination);⑤治疗性疫苗(EGFR v Ⅲ)。以上治疗进展都非常快,如抗免疫检查点抗体药物纳武单抗和帕博利珠单抗,上市不到两年,就进入药物销售TOP 10。
免疫治疗在2013 被《科学》杂志评选为世界十大科技突破之首。2014 年《时代周刊》封面有一句重要的话:“免疫疗法是一种残酷选择性的、昂贵的、拯救生命的疗法”。免疫治疗+ 是未来肿瘤治疗的发展趋势,从化疗药物、靶向药物,到现在免疫治疗药物不断提高疗效,因此,综合治疗成为肿瘤治疗的趋势。
1.抗肿瘤单克隆抗体药物
肿瘤单抗药物发展迅速,截至2019 年10 月,FDA 与欧盟共批准了87 个抗体药物和11 个Fc抗体融合蛋白药物,其中抗肿瘤单克隆抗体药物26 个。我国也批准了26 个抗体药物,其中10 个是抗肿瘤药物。
2. 抗免疫检查点抗体药物
一个细胞分成两个细胞的时候,是细胞周期调节蛋白CDK 在调控细胞周期。对免疫细胞来说,如T 淋巴细胞,除了受CDK 调控之外,还受两类受体——激活性受体和抑制性受体调控,尤其是抑制性受体,调控T 淋巴细胞功能意义非凡。
T 淋巴细胞上有受体PD-1,肿瘤细胞上有其配体PD-L1。两类细胞长期共存,肿瘤细胞“教化”了T 淋巴细胞,使其从免疫抑制、杀伤功能微进化为免疫耐受。基于这个原理,用PD-1 抗体或PD-L1 抗体,可以封闭免疫耐受信号,恢复T 细胞的免疫抑制和杀伤肿瘤细胞功能。
CTLA-4 与PD-1 是美国德州大学MD 安德森癌症中心的詹姆斯·P·艾利森(James P.Allison James P allision ) 和日本京都大学的免疫学家本庶佑(TasukuHonjo) 发现的,由于他们发现了T 细胞抑制性受体,推动了免疫治疗的进展,2018 年同时获得诺贝尔生理学和医学奖。由此研发了一系列抗体药物,如CTLA-4 单抗——伊匹单抗,已经进入了中国的市场;PD-1 单抗药物FDA 批准了7 个,其中2 个已在我国批准进口(帕博利珠单抗、纳武单抗);我国药监局也批准了三个国产PD-1 单抗药物,分别是特瑞普利单抗、信迪利单抗、卡瑞利珠单抗。PD-L1 单抗药物FDA 也批准了3 个,现在只有阿特珠单抗进入中国市场。总的看来,抗免疫检验点抗体药物发展非常迅速。
PD-1 的应用非常广泛,北美注册了1078 个临床方案,中国注册了264 个临床方案(表5)。

但是PD-1 单抗不是万能的,需要检查分子表型之后,符合dMMR(DNA 错配修复)或者MSI(微卫星不稳定性),这类患者才是有效的,所以大约只有20% 的患者适合用其治疗。
3. 免疫T 细胞治疗
免疫T 细胞治疗近年发展也很快,其中发展最快的是基因工程T 细胞(CAR-T)治疗。
(1)CAR-T 治疗
CAR-T 治疗全名是嵌合抗原受体T 细胞免疫治疗(Chimeric Antigen Receptor T-CellImmuno therapy)。T 细胞表面有受体TCR,受MHC 限制, 所以我们采用抗体基因Fab 代替TCR,重组成CAR 通过慢病毒等载体感染T 细胞,即制备成CAR-T 细胞。近年来CAR-T 疗法使用广泛,中国临床注册268 项,成为全球第一。
美国第23 任FDA 主任Scott Gottlieb 在Kymriah 和Yescarta 批准上市后发表过一个重要的声明,表示“我们正在进入一个新的医疗创新前沿,能够重编患者自己的细胞来攻击致命的癌症,基因和细胞疗法等新技术能够在转化医学和治疗许多难治性疾病方面创造拐点”,推动了全球的免疫治疗。
CAR-T 治疗也存在毒副作用,需要引起重视,比如细胞因子释放综合征(CRS)、CAR-T 细胞相关脑病综合征(CRES)、嗜血细胞性淋巴组织细胞增多症(HLH)、脱靶效应(Off-target ontumor),但就目前研究而言,毒副作用是可以控制的,也已经有了相关经验。
(2)最新进展
在今年3 月份美国癌症研究会(AACR)年会上, 间皮瘤等实体瘤的CAR-T 治疗也取得突破性进展。美国纪念斯隆凯瑟琳研究所PrasadAdusumilli 团队,以间皮素作为靶点制备CAR-T,治疗了21 名恶性胸膜肿瘤的患者,其中GMP 瘤有19 例,转移肺癌的有1 例,转移乳腺癌有1 例,结果有9 名患者肿瘤得到控制。同时与PD-1 联合应用的11 名患者当中有2 名达到了完全缓解。
此外,美国贝勒医学院Meenakshi Hegde和Shoba Navai 团队在CAR-T 治疗肉瘤、宾夕法尼亚大学Carl H. June 团队在CAR-T 治疗胶母细胞瘤等方面都取得了重要进展。
(3)CAR-T 治疗实体瘤需要解决的问题
目前对实体瘤的抑制,CAR-T 治疗需要解决三个问题。一是肿瘤的异质性,抗肿瘤CAR-T 疗法需要选择覆盖率比较广的靶点;二是肿瘤微环境;三是T 细胞递送和引导到肿瘤组织的问题。因此,今年美国AACR 年会上提出下一个CAR-T 治疗的前沿是实体瘤(表6)。

4. 树突状细胞疫苗
随着肿瘤细胞的分裂,它们会产生突变,导致肿瘤细胞独特的修饰或新型肽序列出现,这些新的肿瘤特异性多肽及蛋白称为新生抗原(Neoantigen),具有三个特点:①原来肿瘤细胞没有的、经过突变或修饰新产生肿瘤特异肽段/ 蛋白;②新生抗原必须经T 细胞TCR 特异识别;③与MHC 相容。
5. 肿瘤治疗性疫苗
近年在肿瘤治疗性疫苗方面也有较大进展。2017 年7 月,《自然》杂志同一期发表两篇文章,介绍基于肿瘤新生抗原的个性化治疗疫苗,在黑色素瘤患者治疗中取得成功。UgurSahin 团队结果显示,接种疫苗(一个多表位的多肽)的13 个患者中,8 例肿瘤完全消失且23 个月内无复发,其余5 人在肿瘤转移后接种疫苗,2 人出现肿瘤缩小,其中1 人接受PD-1 辅助治疗后肿瘤完全消退。Catherine Wu 团队结果显示,接种疫苗(一个组织相容性的多肽)的6 名患者,4 人肿瘤完全消失,且32 个月内没有复发,另2 人在接受辅助治疗后肿瘤也完全消失。
由上可见,免疫治疗日新月异,未来可期。
四、空军军医大学国家分子医学转化科学中心研究进展
空军军医大学国家分子医学转化科学中心位于陕西西安,是《国家重大科技基础设施建设中长期规划(2012~2030 年)》优先建设的5 个国家级转化医学中心之一,重点建设分子诊断、分子影像及个体化治疗3 个分子医学转化研究平台,并建设分子医学临床检测等7 个功能中心。
长期以来,该中心在肿瘤细胞生物学行为调控和免疫相关介导机制基础研究方面处于领先地位,在新靶点抗体药物和免疫细胞治疗制剂/ 药物方面取得了重要突破。首次解析了CD147 胞外段的晶体结构,并获得了三个新表位(肿瘤、炎症、病原受体)的复合结构。建立了抗体人源化及产业化,人源化嵌合模式动物药物评估体系,免疫细胞重编程等关键技术平台。成功研发13 项抗体药物及免疫细胞治疗产品。2 项产品上市(国家一类新药利卡汀,免疫检测盒凯美汀),4 项进入临床(抗肺癌美妥珠单抗注射液,抗肝癌CAR-T,抗胶质瘤CAR-T,抗肿瘤BSG-TAA DC 疫苗),1 项被FDA 批准为罕见病用药(抗恶性疟疾美珀珠单抗注射剂)。3 次获得全国医药卫生/ 中国医药生物技术十大进展。近5 年来在《肝脏病学》《血液》等国际重要杂志发表130 余篇论文,尤其是今年8 月在《自然》杂志上发表了肿瘤细胞铁死亡新机制的发现,推动了肿瘤治疗的进展。
结语
医学和信息科学技术的进步,为疾病类型重新细分、发现更多的治疗靶点提供了契机。可以预见,以CAR-T 和靶向抗体药物为代表的个体化免疫治疗将为肿瘤等难治性重大疾病的治疗带来革命性的转变,为人类健康保驾护航。
作者介绍

陈志南,1952年6月2日出生于江苏无锡,细胞生物学与生物药物专家,中国工程院院士,中国人民解放军空军军医大学教授、博士生导师,国家分子医学转化科学中心主任 。1979年从陈志南第四军医大学毕业后,留校工作;1989年获得第四军医大学硕士学位;2000年担任第四军医大学基础部细胞生物学教研室主任,细胞工程研究中心主任;2003年获得第四军医大学博士学位;2007年当选中国工程院院士 。陈志南长期从事炎-癌相关分子CD147系列研究。
参考资料
[1]微信公众号中国食品药品监管杂志(ID:zgspypjg),周末文摘 | 新时代生物医药前沿与创新
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn