

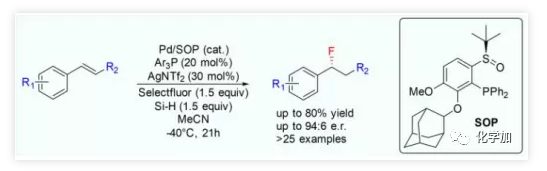
向有机分子中引入氟原子是调节其理化性质、亲脂性和代谢稳定性的重要手段。催化不对称氟化即构建手性 C(sp3)-F键是合成手性含氟分子的有效策略。近年来,烯醇酯或其等价物的α-氟化、C(sp3)-H键的氟化、张力杂环的开环、烯丙基氟化、氟代脱硅、烯酰胺的氟化以及烯烃的氟双重官能团化等取得了重大进展。过去十年中,廉价易得的烯烃的氢氟化已成为构建C(sp3)-F键的重要策略,并引起了广泛关注。目前,常用的氢氟化策略是通过氟阴离子(F-)进攻烷基阳离子(Scheme 1,i)或氟阳离子(F+)进攻烷基自由基(Scheme 1,ii)构建C(sp3)-F键,但其不对称合成仍然充满挑战。
最近,Gouverneur课题组报道了一种新型钯催化的烯基芳烃的氢氟化反应,其通过Csp3-[Pd(IV)(Ln)]-F中间体的还原消除构建出C(sp3)-F键(Scheme 1,iii),这是首例烯烃的催化不对称氢氟化报道。利用Pd/(R)-T-BINAP络合物为催化剂、XeF2为氟源获得手性产物的收率为34%(ee 36%)。与过渡金属催化的烯烃的不对称氢官能团化相比,烯烃的不对称氢氟化研究相对落后,主要是缺乏与氟化试剂相容的催化剂。此外,在Pd(II/IV)催化中,手性Csp3-[Pd(IV)(Ln)]-F中间体的形成通常需要导向基团的辅助。因此,急需开发一种有效的催化体系来解决上述问题。近期,中国科学院成都生物研究所廖建课题组与中南民族大学雷新响课题组团队以Selectfluor®作为氟源和氧化剂、三正己基硅烷作为氢源、(R)-SOP配体为手性源以及三芳基膦作为次要配体实现了钯催化下烯基芳烃的不对称氢氟化(Scheme 1,iv),该成果发表于近期ACS Catal.(DOI: 10.1021/acscatal.9b05264)。
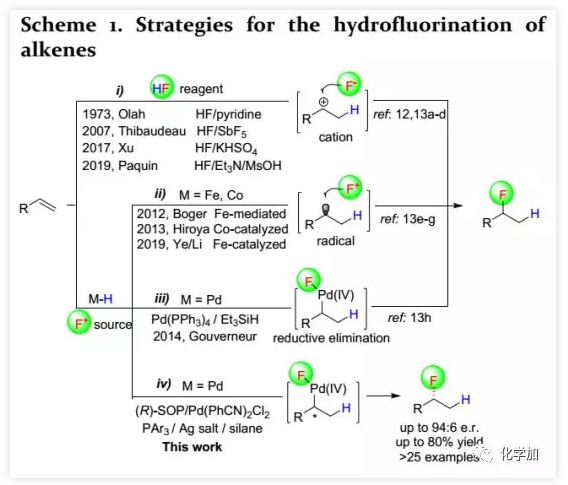
(图片来源:ACS Catal.)
首先,作者选择4-乙烯基联苯(1a)作为模型底物研究了催化不对称氢氟化(Table 1)。在Pd(PhCN)2Cl2(10 mol%)、手性SOP(L1,12 mol%)、三苯基膦(20 mol%,次要配体)、AgNTf2(30 mol%)、三正己基硅烷(1.5 eq.)和Selectfluor®(3.0 eq.)存在下,在-40 ℃乙腈中反应21 h可以良好的收率(80% NMR收率)得到氢氟化产物2a(90.5:9.5 e.r.)。其中,AgNTf2对反应至关重要,其将钯络合物从中性转化为阳离子形式使反应顺利进行;不加银盐时,未检测到2a,只以11%的收率得到还原产物3a。通过对氢源的考察发现,硅烷的性质对对映选择性和收率有影响,这可能是由于硅烷与SOP的Lewis碱(SO)部分的配位所导致,其中三正己基硅烷效果最佳。手性亚砜-(P-二烷基)膦(如L2)不利于该转化,而含有大位阻取代基的P-二芳基膦(L4)可以产生更好的收率和选择性。另外,作者发现使用次要配体对该反应有利。通过对单齿配体(三芳基膦或三烷基膦)、双齿配体和手性膦配体的筛选,发现三(4-甲氧基苯基)膦效果最佳(收率:80%,92.5:7.5 e.r.)。此外,将Selectfluor®用量降至1.5 eq.后,不会影响反应结果。
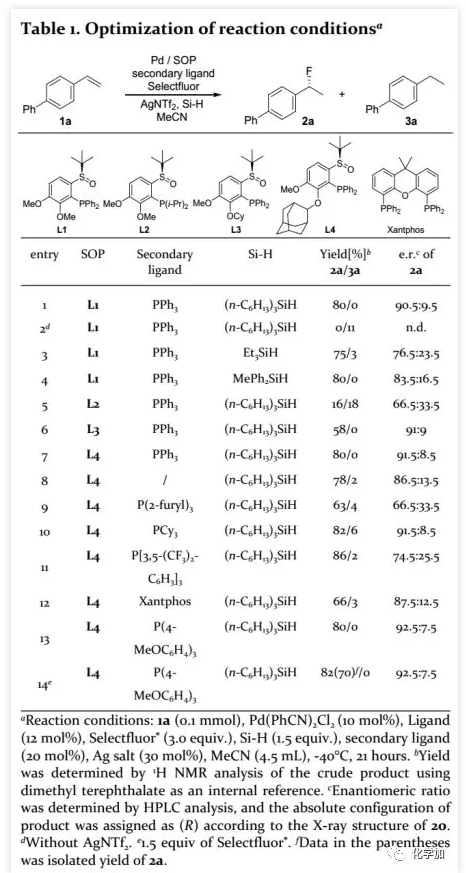
(图片来源:ACS Catal.)
在确定了最佳反应条件后,作者考察了不对称氢氟化的底物范围(Table 2):吸电子和电中性取代基取代的苯乙烯是合适的底物,苯环(联苯)上可以耐受卤素(Cl、F)、甲基、甲氧基和三氟甲氧基等官能团;邻苯基取代的苯乙烯可以41%的收率得到2k(78:22 e.r.);4-(1-萘基)苯乙烯可以73%的收率得到2l(93:7 e.r.);含邻苯二甲酰亚胺基团的底物可以80%的收率得到2o(91:9 e.r.),经两次重结晶后其e.r.值提高至95:5;由雌酮衍生的苯乙烯可以54%的收率得到2p(90.5:9.5 d.r.)。该催化体系还可以耐受其他含不同官能团的取代苯乙烯,包括碘、醚、酯、对甲苯磺酸酯、酰胺和酮,甚至可以耐受含敏感官能团如醛基的底物。此外,2-乙烯基萘可以46%的收率转化为产物2x(88.5:11.5 e.r.),但生成2y和2z的对映选择性和收率均较低。富电子的4-苄氧基苯乙烯生成2aa的NMR收率不足10%。另外,当用脂肪族烯烃如N-(4-戊烯-1-基)邻苯二甲酰亚胺和1-溴-4-(1-苯基乙烯基)苯作为底物时,未产生氢氟化产物。
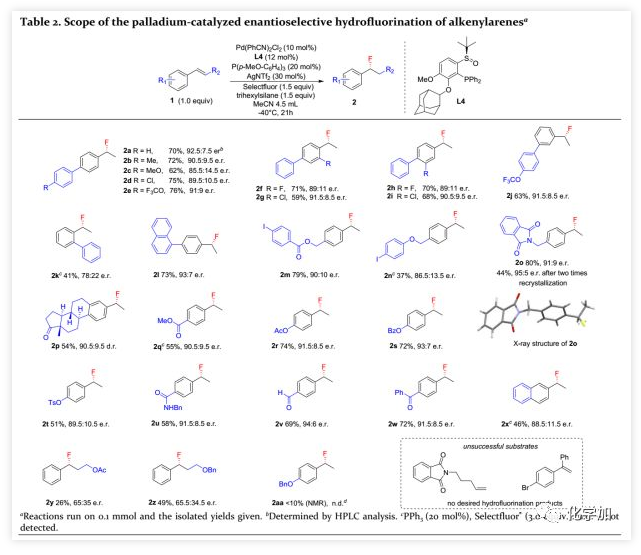
(图片来源:ACS Catal.)
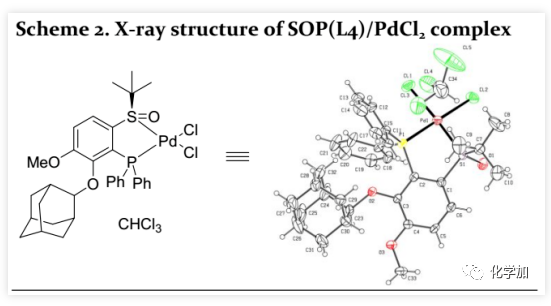
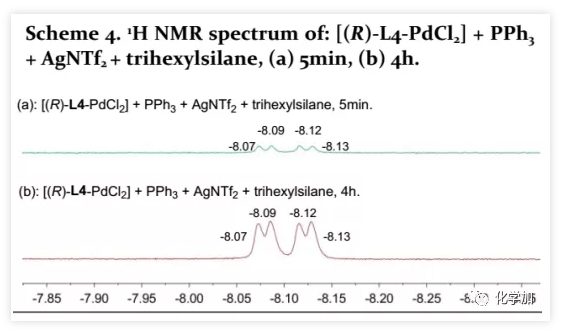
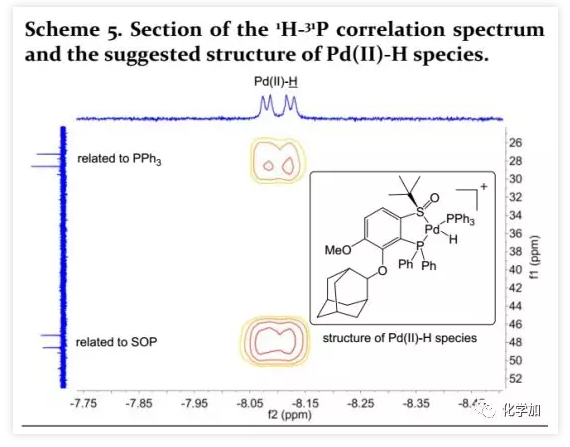
为了研究这种氢氟化的反应机理,作者通过单晶X-射线衍射确定了[(R)-L4-PdCl2]的固态结构,发现SOP的硫和磷原子与钯配位形成五元环(Scheme 2)。为了研究反应过程,作者尝试在-40 ℃氘代乙腈中进行原位一维和二维NMR光谱分析。通过对照实验发现:1)当[(R)-L4-PdCl2]与AgNTf2混合时,31P NMR在56.83 ppm(s)处出峰(Scheme 3a);2)当PPh3与AgNTf2混合时,形成膦-银络合物,31P NMR分别在11.38、11.18、8.65、8.45 ppm处出峰(Scheme 3b);由于磷原子与107Ag和109Ag之间的耦合常数(9.92 ppm, dd, J107Ag31P=615 Hz, J109Ag31P=709 Hz),四个峰成为两个双峰,比率为709/614=1.15,这与两个银同位素的磁旋比关系一致;3)当[(R)-L4-PdCl2]与PPh3、AgNTf2和三正己基硅烷混合5 min时,31P NMR出现两个新峰:47.90 ppm(d, 2JP-P=328.0 Hz)和27.93 ppm(d, 2JP-P=328.0 Hz)(Scheme 3c)。同时,在-8.10 ppm(dd, J=25.3, 7.8 Hz)处观察到Pd-H的信号峰(Scheme 4a);4 h后,31P NMR的信号峰56.84 ppm(s)和9.89 ppm(dd, J107Ag31P =615 Hz, J109Ag31P =709 Hz)移至47.90 ppm(d, 2JP-P =328.0 Hz)和27.93 ppm(d, 2JP-P=328.0 Hz)(Scheme 3d),并且在-8.10 ppm处的信号峰增强(Scheme 4b)。此外,在不存在PPh3时,未观察到氢的信号峰,表明PPh3作为次要配体可以稳定Pd(II)-H。4)二维1H-31P HMBC相关谱显示,31P NMR 上47.90 ppm和27.93 ppm处的信号峰与1H NMR上-8.10 ppm处的信号峰耦合(2JP-P =328.0 Hz, 2JH-P =25.3 Hz, 2JH-P =7.8 Hz)。根据SOP (L4)/PdCl2络合物的单晶X-射线衍射结构和NMR分析,推定Pd(II)-H的结构为[(R)-L4-PdH(PPh3)](P,P trans)(Scheme 5);5)当[(R)-L4-PdCl2]与1a、PPh3、AgNTf2、三正己基硅烷和Selectfluor混合5 min时,发现在31P NMR 的47.90 ppm(d, 2JP-P =328.0 Hz)和27.93 ppm(d, 2JP-P =328.0 Hz)处的信号消失,并56.84 ppm(s)和9.92 ppm(dd, J107Ag31P = 615 Hz, J109Ag31P = 709 Hz)处出现信号(Scheme 3e)。此外,在1H NMR 上-8.10 ppm处的信号消失。结果,观察到(R)-4-(1-氟乙基)-1,1'-联苯(2a)的特征峰在5.73 ppm(dq, J =47.5, 6.6 Hz)和1.64 ppm(dd, J =24.2, 6.4 Hz)。对照实验表明,[(R)-L4-Pd(II)]2+(56.83 ppm,31P NMR)和膦-银络合物(9.92 ppm,31P NMR)可能是催化循环的另一状态。此外,考虑到Pd(II)-H消耗完毕时,仅观察到痕量产物2a。因此,在该催化循环中应该存在另一种存在状态,但实验未观察到。
(图片来源:ACS Catal.)

(图片来源:ACS Catal.)
(图片来源:ACS Catal.)
(图片来源:ACS Catal.)
接下来,作者对1a与Et3SiD的氢氟化进行了评估并得到(2-2H)-2a'为主要产物(Scheme 6),表明硅烷是该催化转化的氢源。

(图片来源:ACS Catal.)
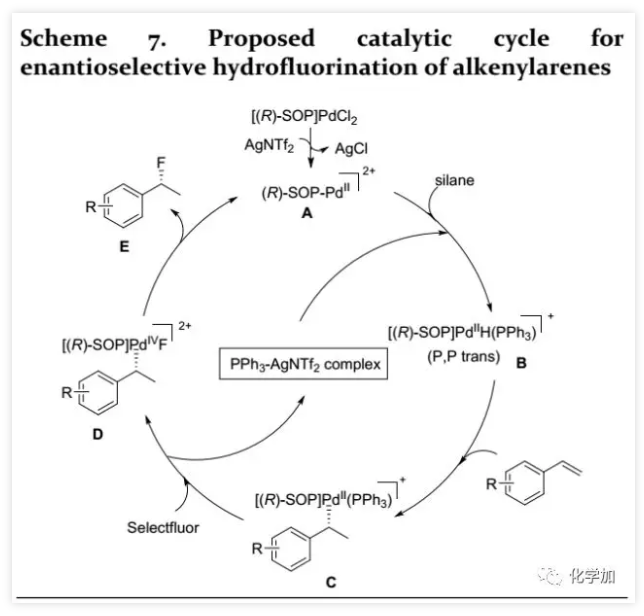
最后,作者提出了该转化的催化循环(Scheme 7):[(R)-SOP-PdCl2]络合物经AgNTf2处理得到阳离子Pd(II)(A);加入硅烷和次要配体(三芳基膦)后促进形成Pd(II)-H(B),其与C=C键配位,并高选择性地在C=C键的Re面插入得到Pd(II)(C);氧化性Selectfluor®将Pd(II)(C)转化为Csp3-[Pd(IV)(SOP)]-F(D);最后,通过Csp3-[Pd(IV)(SOP)]-F(D)的立体定向还原消除生成预期对映选择性的氢氟化产物E。
(图片来源:ACS Catal.)
撰稿人:爽爽的朝阳
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn