

手性醛催化剂作为一种强有力的有机催化剂广泛应用在胺化学当中。因此,高效合成多样性的手性醛催化剂一直是化学家关注的焦点。随着时间的推移,科学家们合成出了多种类型的手性醛催化剂。从早期的Kuzuhara和Breslow教授等人合成的平面手性的仿生吡哆醛环芳烃催化剂,再到后来赵宝国教授发展的脯氨醇衍生的点手性吡哆醛和轴手性吡哆醛催化剂(Scheme 1a)。近期,郭祺祥教授等人发展了一种新型轴手性醛催化剂的方法,主要从手性BINOL骨架出发,历经8-9步左右的转化得到,该类催化剂可用于甘氨酸酯的不对称催化活化反应当中(Scheme 1b)。尽管一些手性醛催化剂的合成已被报道出来,但高效合成双芳基轴手性醛催化剂仍是一大挑战。
近日,浙江大学史炳锋课题组报道了Pd-催化旋转禁阻选择性C-H萘基化合成手性醛催化剂的新策略(Scheme 1c)。该方法连续进行三步C-H键官能团化反应,简单高效构建了轴手性醛催化剂,且产物体现出了优秀的催化性能。
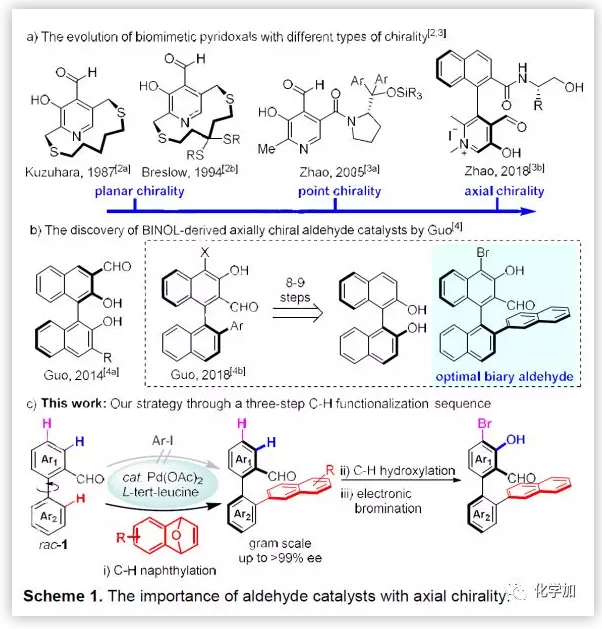
(图片来源:Angew. Chem. Int. Ed.)
如Scheme 2a所示,对双芳基轴手性醛催化剂6进行逆合成分析,化合物6可由5经过亲电溴化得到,5又可以经过3的C-H键氧化得到,而3可以从外消的醛1经过不对称C-H键萘基化得到,共需要三步。但这一方法在优化第一步C-H键萘基化过程出现问题,当选用萘基碘作为芳基化试剂时,尝试大量条件都不能得到化合物3(Scheme 2b)。最后,使用7-氧杂苯并降冰片二烯作为萘基化试剂反应顺利发生,作者提出了可能反应机理:首先底物芳基醛1与手性氨基酸缩合得到亚胺中间体A1和B1;然后对B1进行C-H键活化得到中间体C1,随后发生2a的迁移插入得到中间体D1,b-氧消除得到中间体E1,质子化释放出催化剂得到F1,最后脱氢芳构化得到目标化合物3(Scheme 2b)。
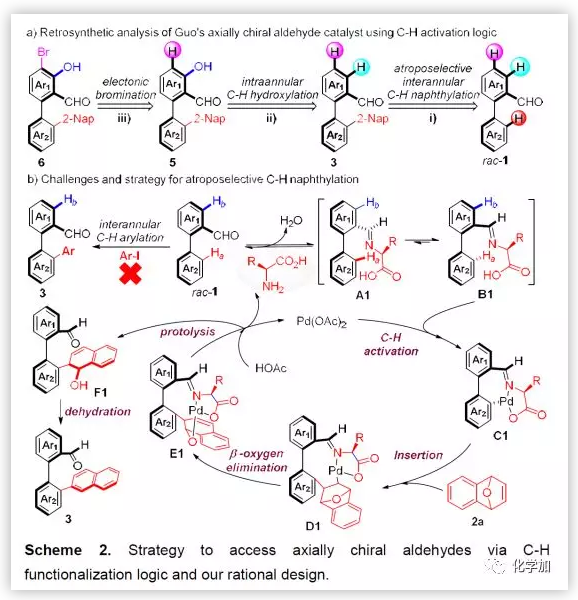
(图片来源:Angew. Chem. Int. Ed.)
为了验证以上设想,作者以rac-1a和7-氧杂苯并降冰片二烯为模板底物、Pd(OAc)2为预催化剂,L-叔亮氨酸为手性配体,在60 oC条件下进行条件筛选。首先对常规的溶剂进行筛选(DCE, THF, Dioxane, Toluene, HFIP, TFE等),发现单一溶剂能以高达99% ee得到目标化合物,但产率仅为13%(Table S1,entry 5)。随后当使用TFE/HOAc混合溶剂时,发现产率提高到32%(Table S1,entry 8)。该现象说明有机酸的加入对反应的活性起到了促进的作用,因此紧接着对一系列的有机酸进行考察。最后发现,当添加金刚烷乙酸和nPrCO2Na时能以71%的产率和>99%的ee值得到3a(Table S1,entry 13)。
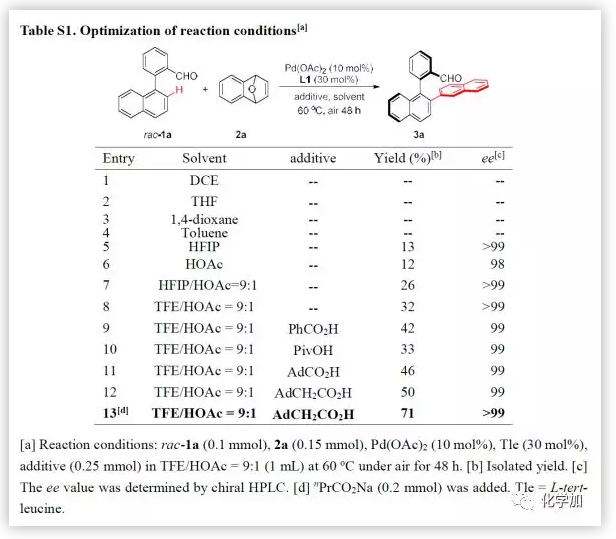
(图片来源:Angew. Chem. Int. Ed.)
在最佳条件下,作者考察了C-H键萘基化反应的底物范围(Table 1)。结果表明,底物rac-1的联芳基片段对吸电子和供电子基团均有良好的兼容性(-OMe, -CF3, -Me,-F, -Cl, and -SPh)(3b-3s)。值得注意的是,当Ar2基团为苯基对位含有取代基时,还可以通过去对称化的过程实现轴手性双芳基化合物的合成(3t-3v)。作者还对底物2的普适性进行考察,使用该方法同样能得到目标化合物3w-3z。其中非芳构化产物3y和3z的产生进一步证实了反应过程可能经历理想模型中F1中间体。
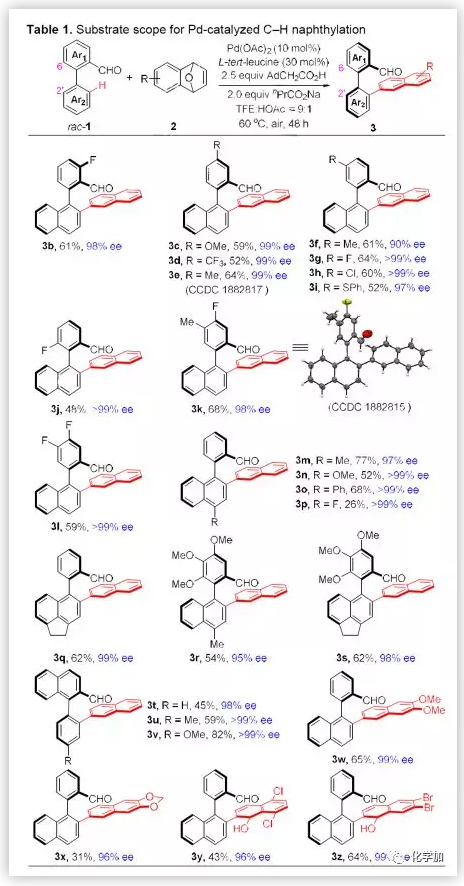
(图片来源:Angew. Chem. Int. Ed.)
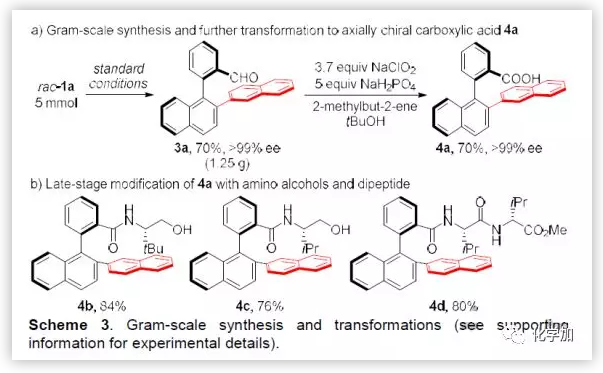
在最优条件下,以70%的产率和>99%的ee值完成了3a的克级规模制备,进一步氧化以对映选择性保持的结果得到轴手性芳基酸4a(Scheme 3)。随后,使用氨基醇和二肽类化合物对4a进行修饰,缩合得到一系列的轴手性酰胺类配体4b-4d(Scheme 3)。这种新型手性骨架有望作为肽基催化剂进行催化应用。
(图片来源:Angew. Chem. Int. Ed.)
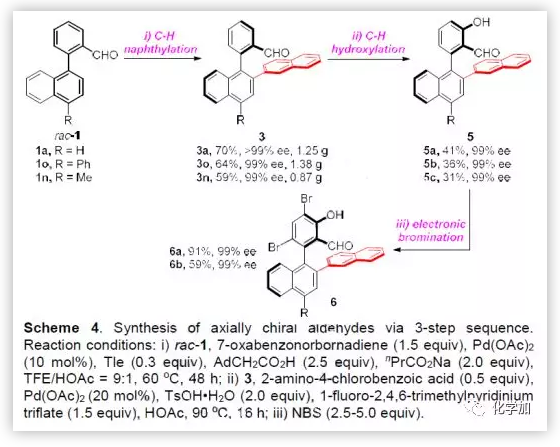
随后,作者尝试了连续的三步C-H键官能团化反应,合成轴手性醛催化剂6(Scheme 4)。反应从双芳基醛底物rac-1出发,经由C-H键萘基化、C-H键羟基化以及亲电溴化完成了轴手性醛6a-6c的合成(up to 91%产率,99% ee)。其中,第二步的C-H键氧化过程非常关键,反复文献调研发现,当对Sorensen教授所报道的条件进行调整后可以有效避免醛基的转化,能够顺利得到预期的氧化产物5a-5c,并能完成克级规模合成。
(图片来源:Angew. Chem. Int. Ed.)
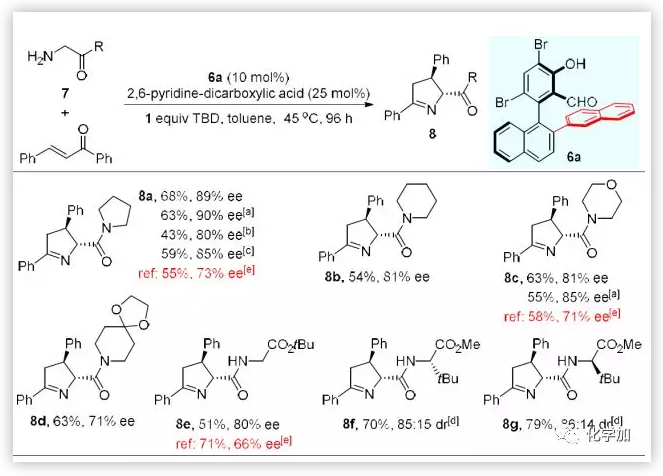
最后,作者将上述合成的轴手性醛催化剂6a运用到查尔酮与甘氨酸衍生的酰胺与二肽类底物7的不对称反应当中(Scheme 5)。郭祺祥教授所报道过的反应中,这一胺类底物7的反应活性较低,得到的产物的对映选择性不理想。对比发现,当使用6a为催化剂时,能够顺利发生反应得到手性吡咯啉衍生物8,且产物8a、8c以及8e都能得到比文献报道更优的产率和对映选择性,说明作者所合成的这一类新型的手性醛催化剂具有一定的优势。
(图片来源:Angew. Chem. Int. Ed.)
总结:浙江大学史炳锋教授课题组报道了Pd-催化旋转禁阻选择的C-H萘基化合成手性醛催化剂的新策略(Scheme 1c)。该策略简单高效,仅需连续三步C-H键官能团化反应即可构建一系列轴手性醛催化剂。进一步的研究表明,该类催化剂在较低活性胺底物中体现出了更优的催化性能。
史炳锋教授课题组:https://person.zju.edu.cn/bfshi/617422.html
撰稿人:莫非
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn