

过渡金属催化烯烃的双功能化已成为快速获得有价值复杂分子的基本策略,电子无偏烯烃的区域选择性是这一领域的一大挑战。化学家们为了解决这个问题,设计了分子内体系,或者在烯烃底物上引入配位基团。相比之下,完全由催化剂控制的三组分转化仍未得到充分研究。
烯烃的烷基化硼化反应在构建C(sp3)-C(sp3)化学键的同时引入了硼基团,为后续的多样化提供了巨大的机会,特别是在铜催化方面取得了重大进展(图1a)。例如,Sawamura和Ito课题组分别使用分子内策略,合成了具有张力的小环。Yoshida课题组利用苯乙烯和电子偏置烯烃研究了分子间的反应。最近,傅尧课题组发展了在弱配位基团的协助下,未活化端烯的1,2-和2,1-烷基化硼化反应(图1b)。然而,在没有配位基团的情况下,未活化烯烃的区域选择性烷基化硼化仍然是一大挑战。近日,武汉大学高等研究院阴国印课题组报道了无配位基团的镍催化电子无偏末端烯烃的1,1-烷基化硼化反应,以高效和高选择性的方式得到二官能化产物(图1c)。在非常温和的条件下,可利用廉价硼试剂,从容易获得的末端烯烃和苄基/烯丙基卤化物合成有用的二级脂肪族硼酸酯。
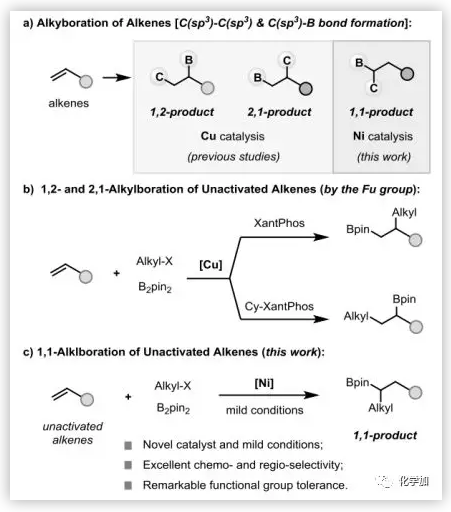
图1. 过渡金属催化的烯烃烷基化硼化反应(图片来源:Angew. Chem. Int. Ed.)
在铜催化的烷基化硼化反应中,从烯烃迁移插入到Cu-B键和随后的键形成中产生的瞬时烷基-Cu中间体主要受益于d10金属难以进行β-H消除。由于一直致力于镍催化的研究,特别是在镍催化烯烃迁移芳基化硼化成功后(Angew. Chem. Int. Ed. 2019, 58, 4612-4616),阴国印课题组推测如果用镍代替铜催化剂,快速的β-H消除和迁移插入将生成稳定的R-CH(Bpin)Ni(II)物种,随后与烷基亲电试剂形成C(sp3)-C(sp3)键,将得到1,1-烷基化硼化产物。
作者首先以端烯1a、苄溴2a和双(频哪醇)二硼(B2pin2,3)的三组分反应为模型反应,对反应条件进行了考察。如图2所示,许多在镍催化中常用的配体都没有或仅得到了痕量的目标产物4a。当采用不寻常的吡啶基酰胺L8时,1,1-烷基化硼化产物4a的收率为69%,进一步优化能使产率提高到91%(L9)。L9和L10的对比表明,吡啶环氮原子邻位的甲基取代基是非常重要的。用L9制备了一种友好、空气稳定的镍配合物,也得到了类似的分离产率。
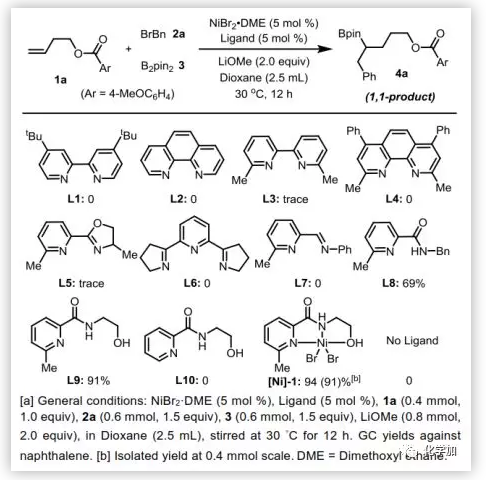
图2. 反应条件筛选(图片来源:Angew. Chem. Int. Ed.)
有了最佳反应条件,作者对这种镍催化反应的底物范围进行了考察。如图3所示,含有多种官能团包括酯、醚、酮、酰胺、氰基、醇、对甲苯磺酸酯、环氧以及官能化的噻吩、吡咯和吲哚的未活化端烯,均能成功地转化成相应的芳基硼化产物,产率良好至优秀,且具有优异的区域选择性(rr>20:1)。以1-庚烯(4b)为原料,合成了1,1-烷基化硼化产物,表明区域选择性受催化剂而不是配位基团的控制。6-溴己烯(4n)的反应中,没有生成环化产物。高烯丙基溴的双键也能以良好的收率得到烷基化硼化产物(4e),此外,含有多个双键的底物中,与单取代烯烃(4s-4v)的选择性反应表明该反应在不同类型的双键间具有良好的化学选择性。为了进一步证明该方法具有良好的相容性,作者还合成了具有生物活性的复杂分子(4w和4x)。值得注意的是,α,β-不饱和酮在镍催化体系(4w)中也具有良好的耐受性。
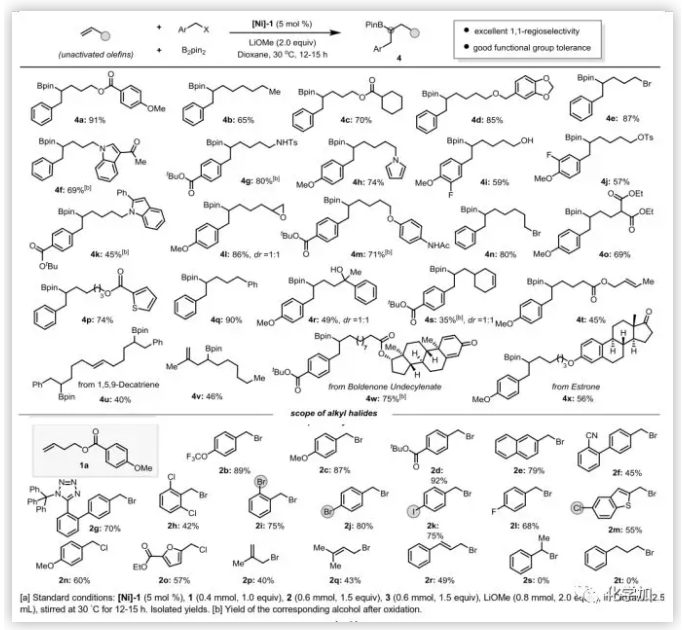
图3. 底物扩展(图片来源:Angew. Chem. Int. Ed.)
为了进一步评估这些催化条件的普适性,作者对一系列取代的苄基溴化物进行了研究,富电子取代基和缺电子取代基对反应活性影响不大。在这种温和的镍催化条件下,芳基氯、溴甚至碘化物都具有良好的耐受性,为进一步的交叉偶联做好了准备。此外,杂环苄基溴化物和苄基氯化物也是适宜的底物(2m-2o)。烯丙基溴代物虽然比苄基卤化物的活性稍低,但在相同的反应条件下也能生成相应的高烯丙基硼酸酯,具有优异的1,1-区域选择性(2p-2r)。但在这些反应条件下,二级苄基溴代物(2s)和未活的化烷基溴化物(2t)不能得到产物。
除了脂肪族烯烃外,在标准条件下,各种芳基乙烯也可以进行烷基化硼化(图4),但在这些反应中只分离出1,2-产物,和Yoshida的铜催化体系结果一致。这可能是由于苄基镍中间体的稳定性所致。
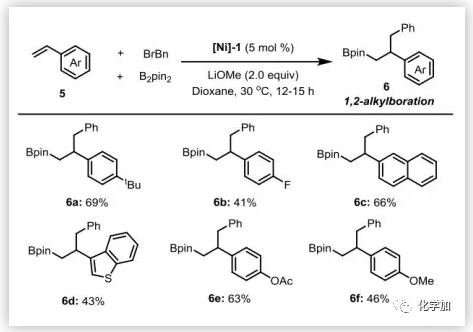
图4. 乙烯基芳烃的反应(图片来源:Angew. Chem. Int. Ed.)
为了深入了解该体系的区域选择性,如图5所示,作者对烯丙基苯和其他几个烯丙基取代官能团进行了研究。烯丙基苯的反应中,1,1-产物7仍占主导地位,其区域异构比为6:1。作者进一步探讨了酯、酰胺和氰基的α-位与硼的α-位之间形成键的能力,发现这三种反应都以良好的选择性得到了1,1-双官能化产物。这表明良好的区域选择性是由新的催化剂决定的。
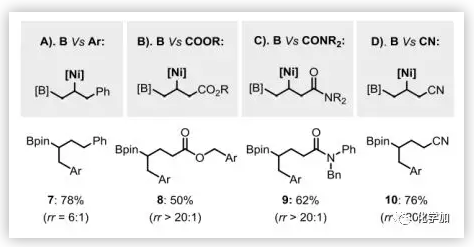
图5. 区域选择性的研究(图片来源:Angew. Chem. Int. Ed.)
为了进一步探索1,1-烷基化硼化反应的潜在范围,作者还使用了气体乙烯。如图6a所示,在气球压力下,当催化剂负载量为1 mol%时,在10 mmol的范围内,能以61%的收率得到产物11。
最后,作者进行了一系列实验来阐明这一转化的机制。首先,用电子顺磁共振(EPR)技术对反应进行监测时,未检测到任何信号,表明催化剂的静态为Ni(0)或Ni(Ⅱ)。在最佳反应条件下,1,1-二硼化合物与2a反应中未观察到Suzuki-Miyaura交叉偶联产物,这排除了1,1-二硼化合物12作为该烷基化反应的中间体的可能性。此外,作者还制备了一种末端氘标记的烯烃[d]-1a,并在反应中进行了考察。产物([d]-4a)的产率为90%,D-原子迁移到β-位的产率为53%。此外,在1a的反应中加入乙烯基硼酸酯13,对反应效率没有影响,也没有检测到氢烷基化产物(14)的形成。这表明,镍迁移参与了这一转化,在迁移过程中,镍氢物种与中间产物不分离。据此,作者提出了1,2-镍迁移的催化循环。如图6e所示,该反应是由Ni(II)物种(I)启动的,它与B2pin2进行转金属化,生成Ni(II)-Bpin物种(II)。随后烯烃迁移插入生成烷基镍(II)中间体(III)。β-H消除得到镍配合物IV,快速迁移插入后得到一个新的稳定的烷基Ni(II)中间体(V),它与活化的烷基卤化物(2)反应,产生1,1-双功能化产物(4)。中间体V与烷基卤化物的反应可能涉及自由基链过程,但在此阶段还不能排除另一种可能涉及双镍的转金属化的可能性。
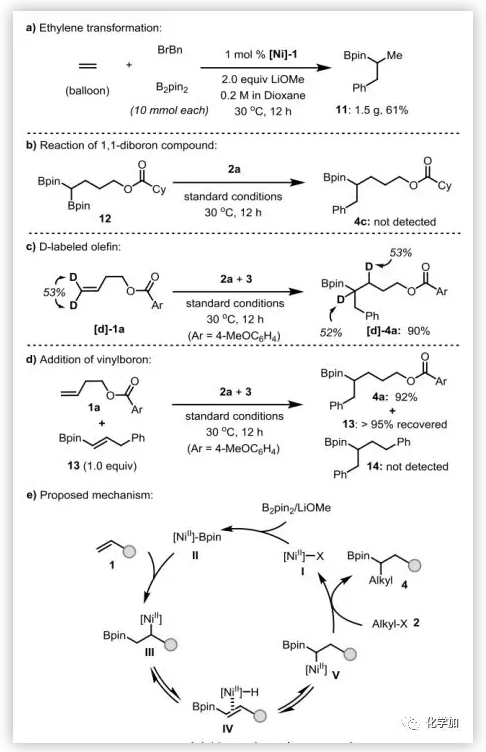
图6. 乙烯的反应及机理研究(图片来源:Angew. Chem. Int. Ed.)
总结:武汉大学高等研究院阴国印课题组采用一种不寻常的吡啶酰胺配体,开发了首例镍催化烯烃的区域选择性1,1-烷基化硼化反应。在非常温和的条件下,以易得的端烯、苄基或烯丙基卤化物和B2pin2为原料,有效地合成了一系列二级烷基硼化合物。更重要的是,这种反应表现出了极好的区域选择性和广泛的官能团相容性,这将大大促进烯烃的转化和烷基硼化物的合成,在有机合成领域具有重要应用价值。
撰稿人:诗路化语
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn