

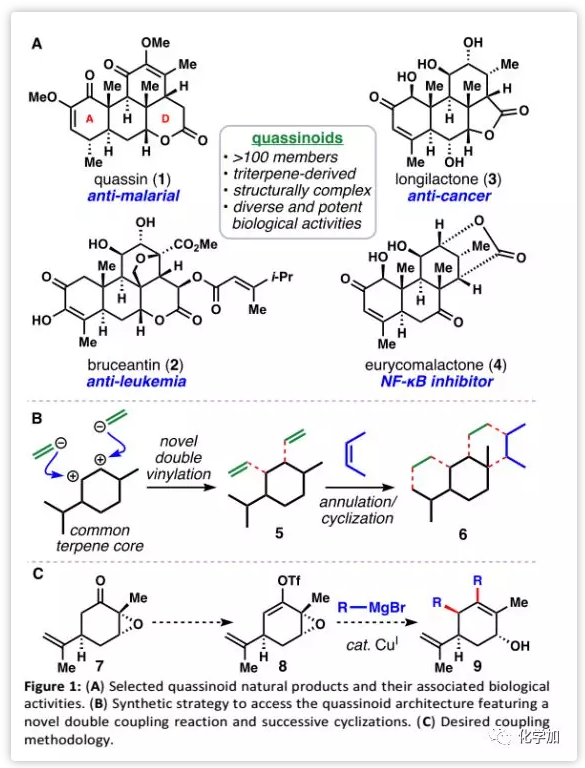
快速构建复杂天然产物分子一直是有机合成的主要推动力,特别是对于高度复杂天然产物的合成简化。苦味碱类天然产物,由三萜衍生而来,其结构特征在于通常含有一个D-环内酯的四环体系(1-4, Figure 1A)。此外,许多苦味碱类天然产物具有显著的生物学特征-特别是有效的抗癌活性。因此,该类天然产物分子一直是有机合成化学家的合成目标。
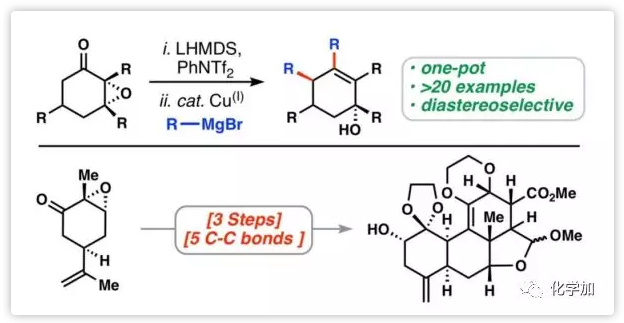
由于先前已经确定了一种手性源单萜的双重乙烯基化转化途径,加州大学伯克利分校Thomas J. Maimone教授课题组设想通过两个连续的成环反应将中间体推进到苦味碱环体系(6)(Figure 1B)。受Wender课题组关于环氧烯醇醚、烯醇磷酸酯和SN2'反应中烯醇化物的各种有机金属试剂的报道以及McMurry课题组关于乙烯基三氟甲磺酸酯与铜酸盐交叉偶联工作的启发,作者设想开发一种Cu(I)催化的转化过程,可以将香芹酮环氧化物7通过乙烯基三氟甲磺酸酯8和简单的格氏试剂直接得到官能化的环己烯醇9(Figure 1C)。近日,Maimone课题组在Chemical Science报道了由Cu(I)络合物催化的环氧酮与格氏试剂的双重偶联,利用该反应只需三步即可形成五个C-C键实现苦味碱母核骨架的构建。
(图片来源:Chemical Science)
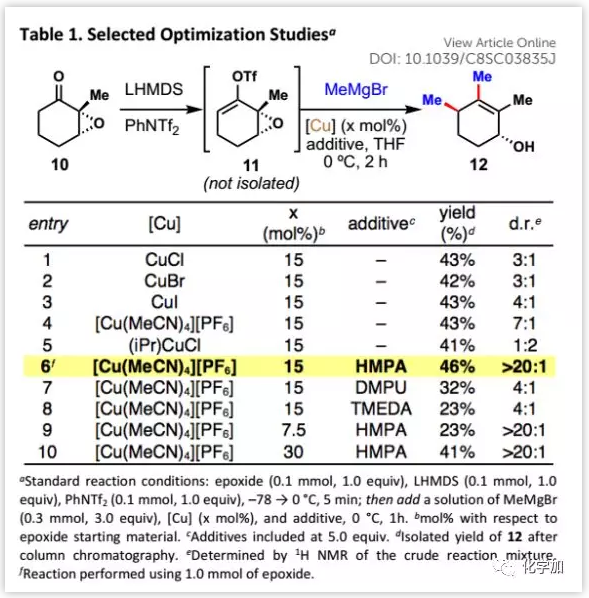
首先,作者用环氧酮10与甲基格氏试剂偶联制备双重偶联产物12作为模型反应进行了研究(Table 1)。其中,乙烯基三氟甲磺酸酯中间体11无需分离;随后,作者发现虽然非对映选择性水平不同,但多种Cu(I)盐均能够催化这种转化。大多数Cu催化剂能够实现烯丙基取代的预期反式立体化学;然而,当Cu中心与庞大的NHC配体连接时,却得到顺式立体化学。在所有铜源中,[Cu(MeCN)4][PF6]效果最好,被用于进一步研究。
极性添加剂可能会影响非对映选择性,特别是发现HMPA几乎将烯丙基全部变为反式异构体。改变催化剂负载量对非对映选择性没有明显影响,但当负载量低于15 mol%时,则对产率产生不良影响。
(图片来源:Chemical Science)
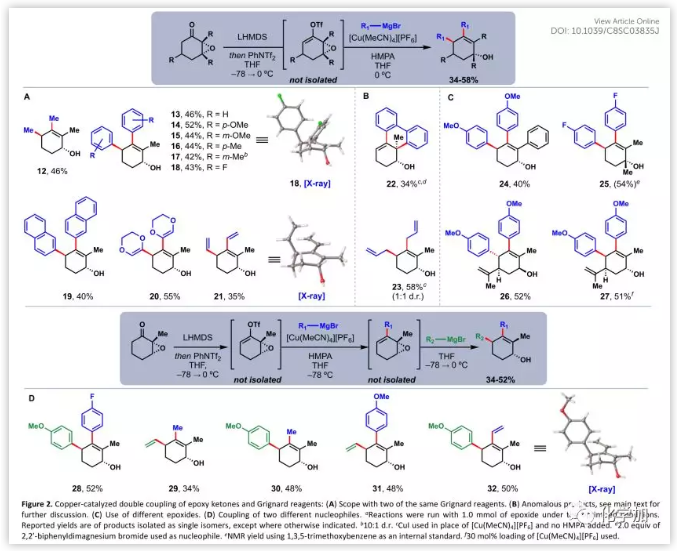
接下来,作者开始探索这种串联偶联过程的适用范围(Figure 2A)。通过实验发现,具有不同取代基的芳香格氏试剂利用该转化可以高纯度和收率得到相应的产物,其他与苦味碱合成有关的sp2亲核试剂如二烯醇基和乙烯基也可以偶联产生单一非对映异构体,18和21的单晶X射线衍射分析证实了反式立体化学。以下两种底物需要指出(Figure 2B):首先,由于可能是分子内的或非催化的过程,衍生自2,2'-二溴联苯的二格氏试剂时形成的产物22仅经历了环氧化物的交叉偶联和SN2开环;其次,由于试剂的高亲核性,烯丙基格氏试剂的偶联产物23为顺式和反式非对映异构体的1:1混合物。
该方法还可以耐受不同的环氧化物底物(Figure 2C)。用较大的苯基取代2-甲基或在3-位引入甲基不会影响相应的产物生成(24,25)。然而,该化合物的叔烯丙醇片段对酸高度敏感,易发生脱水反应。香芹酮环氧化物的两种非对映异构体也可以干净得到相应的产物(26,27)。另外,该反应可以克服cis-香芹酮环氧化物的固有空间取向得到anti-27。
最后,作者将该方法进行了扩展,通过“一锅法”与两个不同的亲核试剂进行偶联(Figure 2D)。首先,作者发现在低温(-78 ℃)下,可以进行选择性交叉偶联得到产物。当用不同的亲核试剂处理该中间体,仅在加热至0 ℃时才进行烯丙基取代。此外,亲核试剂本身(芳基、乙烯基、烷基等)不会改变这种转化的选择性; 而控制因素是亲核试剂的加入顺序和反应温度。因此,通过改变亲核试剂的加料顺序,可以直接得到区域异构产物31和32,通过单晶X射线衍射分析证实了32的连接和选择性。
(图片来源:Chemical Science)
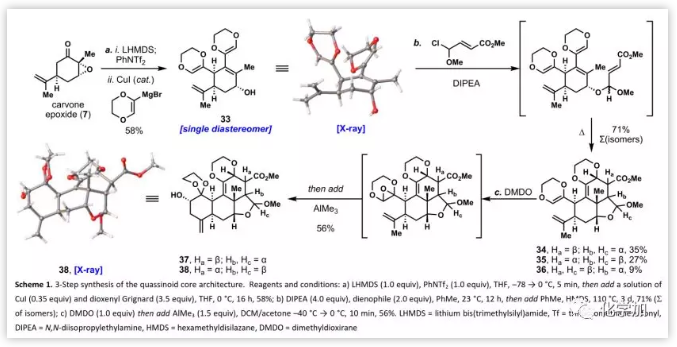
接下来,作者将注意力转向于苦味碱环体系的构建(Scheme 1)。首先,作者将香芹酮环氧化物与基于二烯烃的Grignard试剂偶联得到单一异构体33,通过X射线晶体学分析确定其立体化学为反式。作者认为苦味碱的C-环和D-环可以由乙烯基二氧六环片段与连接在烯丙醇33上的亲二烯醇片段通过分子内Diels-Alder反应构建。由于烯丙醇在热和酸性条件下不稳定,起初的尝试均失败。最后,在碱性(DIPEA)条件下,用甲基氯代烷基醚将游离醇烷基化产生一对非对映异构缩醛(d.r. 1:1),然后加热进行Diels-Alder反应。实验发现,缩醛立体化学对环加成反应的内/外式选择性具有很强的控制作用,即一种缩醛异构体只产生内式产物(34),而另一种产生exo-35优于endo-36(3:1 exo:endo),分离得到两种主要的非对映异构体endo-34和exo-35,其中通过单晶X射线衍射分析证实35为外式产物。
对于苦味碱母核的合成,作者设想通过级联二烯烃氧化/重排/环化构建A环。Hanna及其同事之前报道,取代的二烯烃的环氧化和重排成醛很容易进行。作者在实验中发现,通过用DMDO处理,然后加入Lewis酸可以得到干净的环氧化物中间体(Scheme 1);并且,三甲基铝是两种转化的最佳Lewis酸,可以56%的总产率得到仲醇37和38。随后,以相当的效率得到两种烯产物,并且在新形成的醇立体中心为单一异构体。38的立体化学通过单晶X射线晶体学分析进一步证实。至此,仅通过三步就完成了苦味碱母核结构的构建,其中构建了五个C-C键和七个手性中心。
(图片来源:Chemical Science)
小结:Thomas J. Maimone教授课题组开发了一种新型的铜催化双重官能化反应,将易得的环氧酮转化为高度取代的非对映异构纯的烯丙基醇,并将其用于快速构建(仅三步)苦味碱母核结构中。该转化具有广泛的底物范围,包括各类亲核试剂和环氧化物。作者开发的方法有助于快速获取高价值的中间体和其他复杂的天然产物结构以及合成多种苦味碱类天然产物。
撰稿人:爽爽的朝阳
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn