

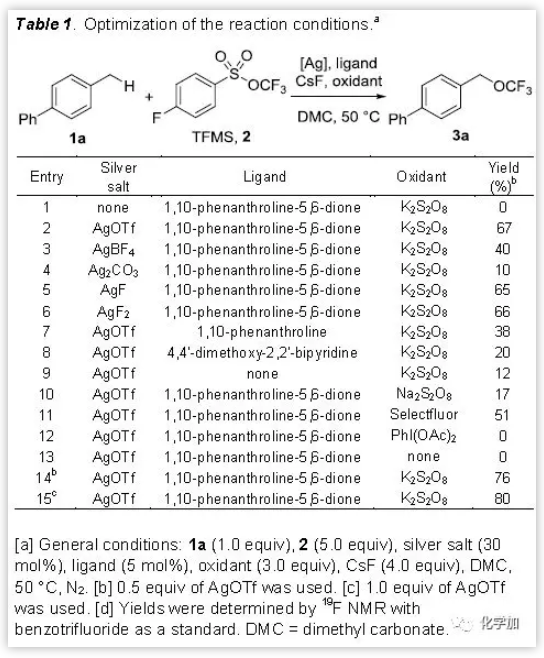
汤平平课题组曾用银催化实现了苄位C-H活化合成芳烃的二氟甲基化,该反应被证明经过了苄基自由基中间体过程。受这一结果启发,本文作者试图尝试使用新型三氟甲氧基化试剂(TFMS)来实现苄位C-H键的直接三氟甲氧基化。如Table1所示,本文作者首先使用4-甲基-1,1’-二苯(1a)与TFMS(2)为模型底物来优化反应条件。通过催化剂筛选发现AgOTf是最好的催化剂,使用该催化剂可以以67%的产率得到目标产物3a,而不加银盐则无目标产物生成(entries 1 to 6)。
此外,配体对该反应的进行也非常关键,1,10-邻二氮杂菲-5,6-二酮做配体的产率最高,而不加配体的条件下产率仅有12%(entries7 to 9)。同时,本文作者还筛选了不同的氧化剂,发现最佳氧化剂为K2S2O8。使用Na2S2O8、选择性F试剂、PhI(OAc)2替代K2S2O8会使产率降低(entries10 to 12),不加氧化剂则没有产物生成(entry 13)。随后,本文作者还对AgOTf的使用量进行了筛选。将AgOTf提升至0.5当量,产率可达76%,化学计量的AgOTf可以让产率达到80%(entry 14, 15)。但是,因为该反应对底物的电子性质非常敏感,在1个当量的AgOTf条件下产率并不总是高于0.3当量AgOTf条件的产率,因此,本文作者使用了0.3当量的AgOTf进行后续研究。
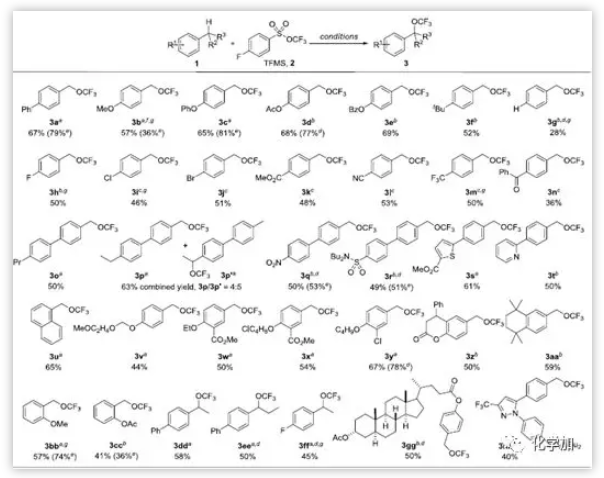
接下来,本文作者进行了Scheme 1所示的底物扩充。不同甲基取代的芳烃(包括具有吸电子、给电子取代的芳烃)均适用于该反应,可以以28%-81%的产率得到相应的三氟甲氧基化产物。但随芳烃上取代基的电负性不同,反应条件要随之调整。例如,具有吸电子取代的底物(1i to 1n),化学计量的AgF2做银盐最佳。F、Cl、Br、醚、酯、酮、氰基以及磺酰胺基在该条件下均耐受。但羟基、氨基和羧基等具有自由氢的底物不耐受,得不到目标产物。当使用甲苯作为底物,产率仅有28%(2g)。杂环底物(1s和1t)同样可以反应。
除了甲基,本文作者发现亚甲基(1dd to 1ff)在该条件下同样可以进行三氟甲氧基化(3ddto 3ff,产率分别是45%,58%)。随后,本文作者使用1o及1p作为原料来探索此三氟甲氧基化反应的选择性。对于底物1o,三氟甲基化主要发生在一级苄位(而非三级苄位)。而使用1p作为底物,一级苄位及二级苄位均会发生三氟甲氧基化,比例为4:5。这一结果证明此三氟甲基化反应活性二级苄位C-H>一级苄位C-H>三级苄位C-H。值得一提的是,更为复杂的底物在此条件下也可成功实现三氟甲氧基化(3gg和3hh),并且,使用该条件可以在产率基本保持的情况下实现克级规模合成。例如,产物3e就可以以70%的分离产率克级制备,这充分显示了该方法的可扩展性。
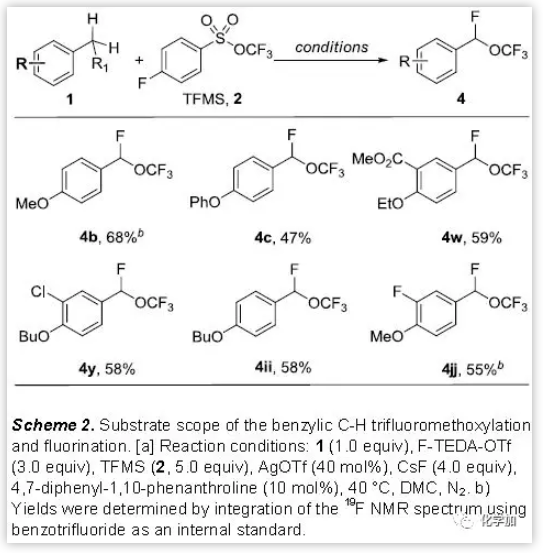
受以上结果激励,本文作者继而关注苄位C-H的双三氟甲氧基化。意外的,当使用F-TEDA-OTf作为氧化剂,得到的主产物是α-氟代苯三氟甲基醚4,而未生成双三氟甲氧基化产物。这种同时在一个位置上引入氟原子和三氟甲氧基的方法鲜有报道。目前为止,未有通过C-H活化活化来实现这类转化的相关报道,因此,本文作者进而对该反应做了进一步探索。
使用优化后的反应条件(40 mol%AgOTf, 10 mol%配体,4当量的TFMS,3当量的F-TEDA-OTf,4当量的CsF,DCM,40 ℃,15 h),产物4b的产率可以达到68%。其他供电子取代的甲苯在此条件下也可以得到相应的F、三氟甲氧基同时取代的产物(Scheme2)。但具有吸电子和电中性的取代基的甲苯作为原料不能发生该类反应,可回收到80%以上的原料。值得指出的是,该反应所得到的产物4很容易在硅胶柱或者氧化铝柱纯化的时候分解产生相应的醛。
接着,作者进行了机理研究。首先,使用化合物1a及其氘代类似物1a’在标准条件下进行动力学同位素效应(KIE)试验。通过19F NMR分析发现,平行试验的kH/kD值为1.4,这说明C-H键的断裂在该反应中并不是决速步。其次,当该反应加入1当量的自由基抑制剂——二丁基羟基甲苯(BHT)或1,1-二苯乙烯,则三氟甲氧基化反应不能进行。而且,当使用底物5作为自由基探针,会得到开环产物6(scheme 3a)。这说明该反应体系存在游离自由基。最后,通过Scheme 3b反应证明该反应是通过先先三氟甲氧基化然后进行F代反应。此外,通过19F核磁谱也观察到了该反应会生成二三氟甲基化中间体,但该类化合物在此反应条件下不稳定,会分解生成相应的醛。
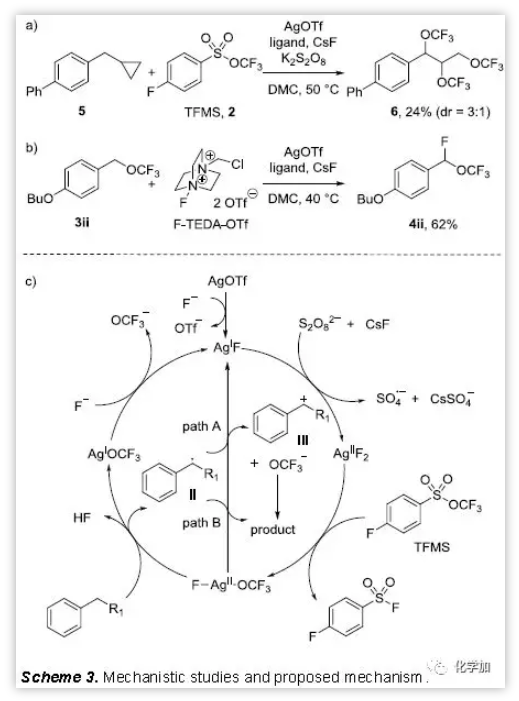
通过机理证明及DFT计算,本文作者提出了scheme 3c所示反应机理。首先,AgOTf在原位经F离子交换得到Ag(I)F,随后在氧化剂作用下氧化生成Ag(II)F2。然后,Ag(II)F2与TFMS作用生成FAg(II)OCF3,该化合物可氧化苄位C-H键产生苄基自由基II。最后,苄基自由基II与FAg(II)OCF3反应生成目标产物(path B)。此外,DFT计算还发现苄基自由基II可以被FAg(II)OCF3氧化产生苄基碳正离子III(path A),该碳正离子也可被OCF3离子捕获得到目标产物。
总结:汤平平教授课题组首次报道了一种银催化的苄位C-H三氟甲氧基化反应。该反应使用TFMS作为三氟甲氧基化试剂,官能团的耐受性广且适合克级规模合成。并且,本文还首次报道了苄位的同时三氟甲基化和F代反应,具有较高的创新性。
原文链接:https://doi.org/10.1002/anie.201807144
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn