

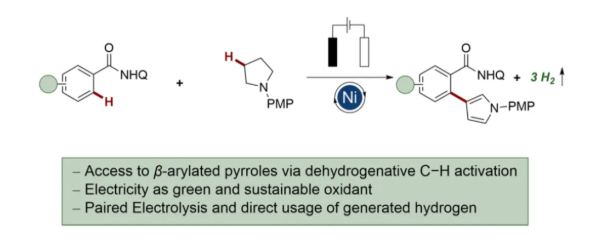
近几十年来,电化学经历了一场复兴,因其作为兼具成本效益与环境友好特性的分子合成工具而备受关注。其显著优势在于能够消除对非理想化学计量氧化还原试剂的使用,从而减少废弃物的生成。此外,通过底物的恒电位控制可实现反应条件的精细调控,并赋予氧化还原电位控制的化学选择性。金属-电催化领域的最新进展已拓展了电化学反应的范围,通过独特的选择性控制实现了具有挑战性的分子转化,包括C-H键活化。在此背景下,与铑或钯等贵金属相比,储量丰富的3d过渡金属因其成本更低、毒性更小的特性,已成为极具前景的催化剂。其中,镍在可持续但高效的C-H键活化催化中展现出卓越潜力。值得注意的是,Chatani等团队在镍催化C-H芳基化反应领域做出了关键性贡献。另一方面,β-芳基吡咯结构单元广泛存在于各类天然产物和药物化合物中(Scheme 1a)。然而,β-芳基吡咯的合成仍然具有挑战。前期研究表明,通过精心的催化剂和配体设计,可实现相应的β-选择性,从而实现了吡咯的官能团化。然而,此类方法通常依赖于昂贵的贵金属催化剂,如铑或钯。此外,为了抑制不期望的α-芳基化反应,通常需要2,5-二取代基团,而非活化吡咯的β-芳基化仍然很少见,且尚未得到充分的探索(Scheme 1b)。近日,德国哥廷根大学Lutz Ackermann团队报道了一种前所未有的镍电催化脱氢C-H活化合成β-芳基吡咯的方法(Scheme 1c)。该研究的主要创新点包括:a)实现了复杂β-芳基吡咯的合成;b)通过质子与电子(以电为绿色氧化剂)替代化学计量氧化剂;c)详尽的机理研究;d)配对电解技术;e)多步脱氢过程促进析氢反应(HER)释放氢气;f)克级规模合成,突显了该方法的合成实用性。欢迎下载化学加APP到手机桌面,合成化学产业资源聚合服务平台。
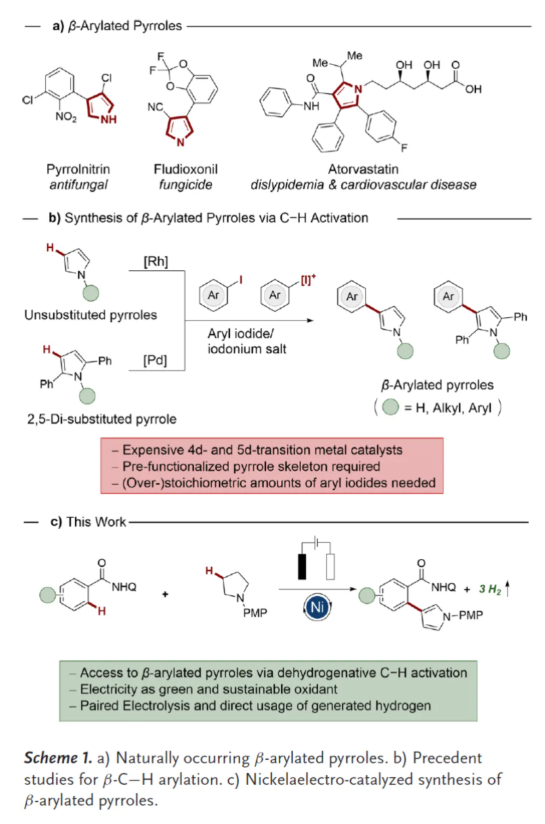
(图片来源:Angew. Chem. Int. Ed.)
其次,作者以苯甲酰胺衍生物1a与吡咯烷衍生物2作为模型底物,进行了相关反应条件的筛选(Table 1)。当以Ni(dme)Cl2(10 mol %)作为预催化剂,TBAPF6(1.6 equiv)作为电解质,NaO2CAd(2.0 equiv)作为添加剂,玻碳(GC)作为阴极,石墨毡(GF)作为阳极,电流为8.0 mA,DMA作为溶剂,在无隔膜电解槽中140 oC反应17 h,可以64%的收率得到β-芳基吡咯产物3。

(图片来源:Angew. Chem. Int. Ed.)
在获得上述最佳反应条件后,作者对底物范围进行了扩展(Scheme 2)。首先,当底物1中的芳基上含有各种不同电性的取代基时,均可与2顺利进行反应,获得相应的产物3-23,收率为25-88%。其中,含有氧化性敏感的硫醚(18)和烯基取代基(19)的底物,均与体系兼容,突显了该策略的化学选择性。其次,苯并噻吩杂环化合物,也是合适的底物,可以70%的收率得到产物24。此外,当底物1中的喹啉基团上含有不同位取代的甲基时,也能够顺利进行反应,获得相应的产物25-27,收率为25-88%。
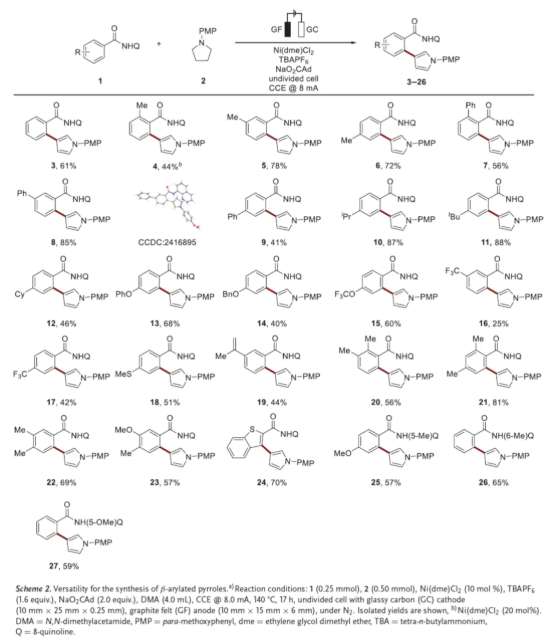
(图片来源:Angew. Chem. Int. Ed.)
紧接着,作者对反应的实用性进行了研究(Scheme 3)。首先,1c和2的克级规模实验,同样可以66%的收率得到产物5(Scheme 3a)。其次,底物1y(其远端位置含有一个额外的烯基),在标准条件下也成功进行了氢化反应,可以60%的收率得到产物28。这一结果凸显了电化学介导反应性的独特优势,即通过同时利用阳极氧化与阴极还原的双重转化路径(Scheme 3b)。此外,作者发现,电流能够调控反应的化学选择性。通过恒电流电解(4.0 mA)可优先生成环化产物29-31(收率为17-24%),这证明了电化学策略的可调性能够揭示传统方法难以触及的新反应路径(Scheme 3c)。最后,通过对所得产物3的进一步衍生化(如氢化反应),可以88%的收率得到氢化喹啉化合物32(Scheme 3d)。
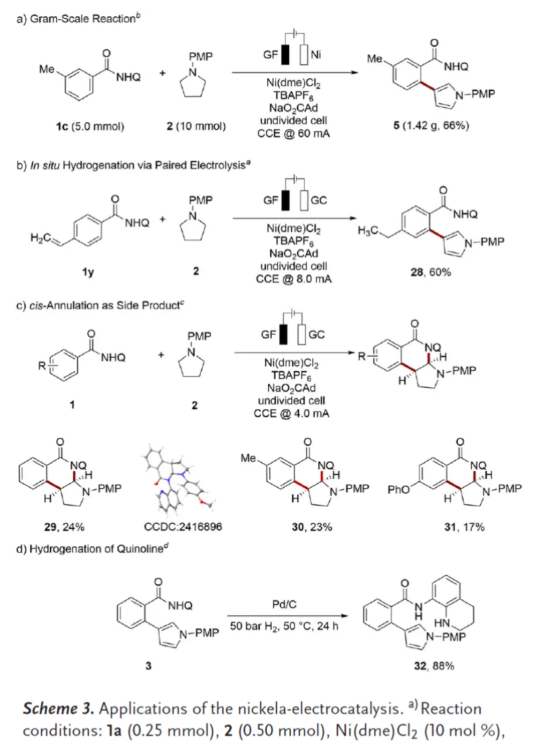
(图片来源:Angew. Chem. Int. Ed.)
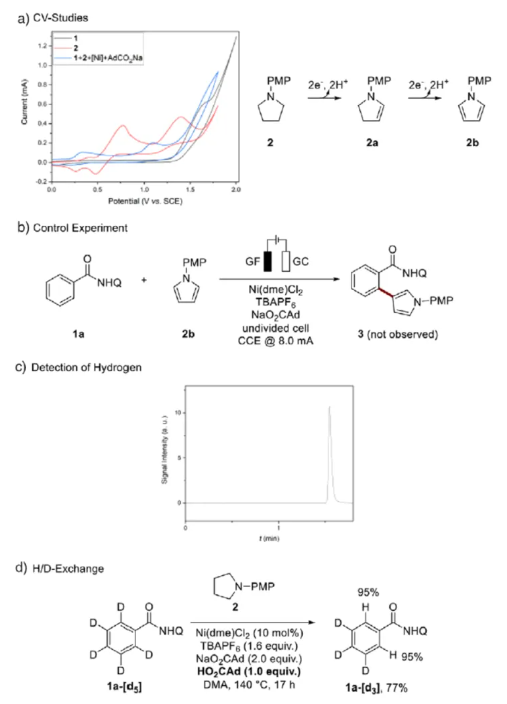
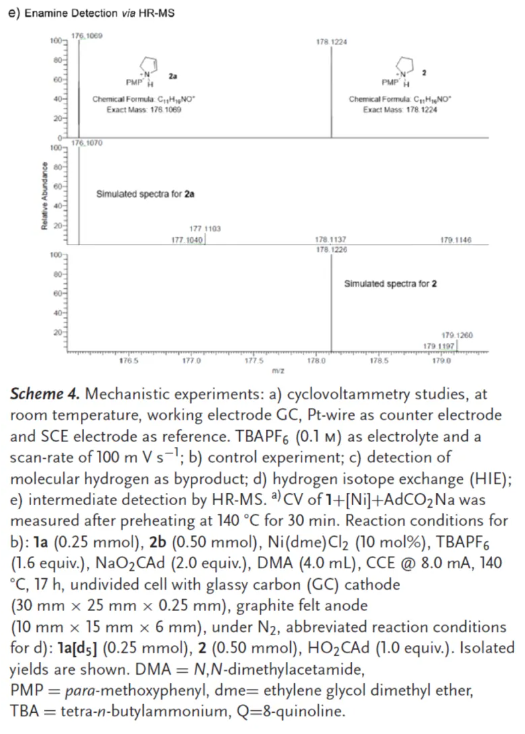
随后,作者对反应的机理进行了研究(Scheme 4)。首先,底物2的循环伏安法(CV)图中观察到两个明显的氧化峰,表明了其可能涉及两步氧化过程,即首先生成烯胺中间体2a,随后进一步转化为吡咯中间体2b。同时,原位制备的镍配合物A在+0.3 V和+1.1 V下表现出两次氧化事件。根据前期研究结果,镍(II)配合物A的电化学氧化分别在约-0.2 V和+0.5 V下生成镍(III)配合物B和镍(IV)配合物C。并且,第二个氧化峰也可能源于吡咯烷与镍催化剂配位后的氧化过程(Scheme 4a)。其次,以吡咯衍生物2b作为底物进行的对照实验,但未获得所需的目标产物3(Scheme 4b)。通过电解过程中顶空气体的气相色谱-热导检测(GC-TCD)分析,确认原位生成了氢气(Scheme 4c)。此外,作者探索了一种无需电力的可行性的氢同位素(D/H)交换(HIE)方法,并观察到高达95%的氢掺入率。因此,羧酸盐辅助的C-H活化过程具有快速且可逆的特性(Scheme 4d)。最后,高分辨率质谱(HR-MS)的详细机理研究表明,烯胺中间体2a(以及烯胺中间体2c)是反应的关键中间体(Scheme 4e)。
(图片来源:Angew. Chem. Int. Ed.)
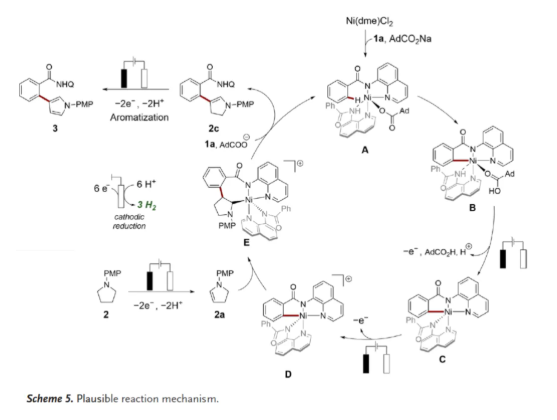
基于上述的研究,作者提出了一种合理的反应机理(Scheme 5)。首先,Ni(dme)Cl₂与苯甲酰胺1a的配位,生成催化活性配合物A。其次,羧酸盐辅助BIES(碱辅助分子内亲电取代)C-H活化,生成中间体B,该中间体经历连续两次电化学氧化,分别得到中间体C与中间体D。同时,吡咯烷2通过PCET过程氧化为烯胺中间体2a,后者与金属环D反应生成中间体E。随后,通过进一步的β-消除,可生成烯胺中间体2c并再生活性配合物A。相比之下,中间体E中C-N的还原消除,则更可能形成环化副产物29。最后,烯胺中间体2c经进一步氧化,从而获得目标β-芳基化吡咯产物3。
(图片来源:Angew. Chem. Int. Ed.)
总结
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn